一定温度下,可逆反应H2+I2 2HI达到化学平衡状态的标志是( )
2HI达到化学平衡状态的标志是( )
 2HI达到化学平衡状态的标志是( )
2HI达到化学平衡状态的标志是( )| A.混合气体的压强不再变化 | B.混合气体的颜色不再变化 |
C.反速率v(H2)=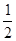 v(HI) v(HI) | D.c(H2):c(H2):c(HI)=1:1:2 |
 2HI达到化学平衡状态的标志是( )
2HI达到化学平衡状态的标志是( )| A.混合气体的压强不再变化 | B.混合气体的颜色不再变化 |
C.反速率v(H2)=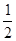 v(HI) v(HI) | D.c(H2):c(H2):c(HI)=1:1:2 |