题目内容
将等物质的量的A、B混合于2L的密闭容器中发生如下反应:3A(g)+B(g) nC(g) +2D(g),经过5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L.min).
nC(g) +2D(g),经过5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L.min).
则(1)n= ;(2)反应开始前容器中B的物质的量为 mol;
(3)5min时A的转化率是 。
 nC(g) +2D(g),经过5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L.min).
nC(g) +2D(g),经过5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L.min).则(1)n= ;(2)反应开始前容器中B的物质的量为 mol;
(3)5min时A的转化率是 。
(1)(2分)2; (2)(3分)3 ; (3)(3分)50℅ 或0.5
C的平均反应速率为0.1mol/(L.min),由此生成C和D的物质的量分别是0.1mol/(L.min)×2L×5min= 1.0mol、0.5mol/L×2L=1.0mol,即C和D的变化量之比是1︰1,所以n等于2。
3A(g)+B(g) 2C(g) +2D(g),
2C(g) +2D(g),
起始量(mol) a a 0 0
转化量(mol) 1.5 0.5 1.0 1.0
平衡量(mol) a-1.5 a-0.5 1.0 1.0
所以 ,解得a=3
,解得a=3
由此A的转化率是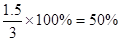 。
。
3A(g)+B(g)
 2C(g) +2D(g),
2C(g) +2D(g),起始量(mol) a a 0 0
转化量(mol) 1.5 0.5 1.0 1.0
平衡量(mol) a-1.5 a-0.5 1.0 1.0
所以
 ,解得a=3
,解得a=3由此A的转化率是
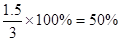 。
。
练习册系列答案
相关题目
 2Z(气)+aQ(气)
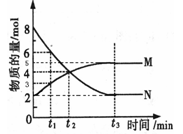
2Z(气)+aQ(气) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示下列判断正确的是
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示下列判断正确的是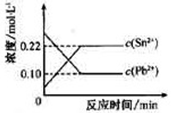
 FeO(s)+CO(g) △H1,平衡常数为K1
FeO(s)+CO(g) △H1,平衡常数为K1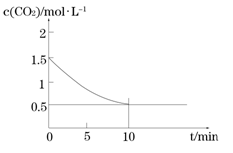
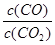 增大的是 (填序号)
增大的是 (填序号)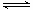 Fe3O4(s)+4H2(g)之后,测得H2O蒸气的分解率为x%,浓度为c1mol/L。若再充人1mol H2O蒸气,建立新的平衡后.又测得H2O蒸气的分解率为y%,浓度为C2 mol/L。则下列关系正确的是
Fe3O4(s)+4H2(g)之后,测得H2O蒸气的分解率为x%,浓度为c1mol/L。若再充人1mol H2O蒸气,建立新的平衡后.又测得H2O蒸气的分解率为y%,浓度为C2 mol/L。则下列关系正确的是 Si3N4 + 6CO,该反应过程中的能量变化如图所示;回答下列问题:
Si3N4 + 6CO,该反应过程中的能量变化如图所示;回答下列问题: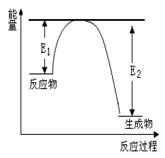
 (正)
(正)  2C在不同温度下经过一定时间,混合物中C的百分含量与温度关系如下图所示,那么:
2C在不同温度下经过一定时间,混合物中C的百分含量与温度关系如下图所示,那么: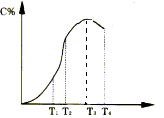 (1)反应在___________________温度下达到化学平衡;
(1)反应在___________________温度下达到化学平衡; Fe(s)+CO2(g) △H="a" kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( )
Fe(s)+CO2(g) △H="a" kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( ) N2O4(g);△H<0,在测定NO2的相对分子质量时,下列条件较为适宜的是
N2O4(g);△H<0,在测定NO2的相对分子质量时,下列条件较为适宜的是