0 104813 104821 104827 104831 104837 104839 104843 104849 104851 104857 104863 104867 104869 104873 104879 104881 104887 104891 104893 104897 104899 104903 104905 104907 104908 104909 104911 104912 104913 104915 104917 104921 104923 104927 104929 104933 104939 104941 104947 104951 104953 104957 104963 104969 104971 104977 104981 104983 104989 104993 104999 105007 203614
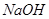 溶液喷淋“捕捉”空气中的
溶液喷淋“捕捉”空气中的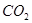 。
。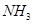 为原料可合成化肥尿素[
为原料可合成化肥尿素[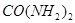 ]。已知:
]。已知:
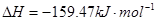 ①
①
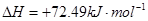 ②
②
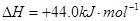 ③
③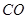 ,在催化剂作用下CO和
,在催化剂作用下CO和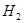 反应生成甲醇:
反应生成甲醇: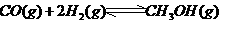 某容积可变的密闭容器中充有10molCO与20mol
某容积可变的密闭容器中充有10molCO与20mol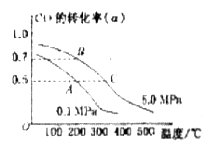
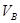 _______VL。(填“大于”、“小于”或“等于”)
_______VL。(填“大于”、“小于”或“等于”)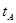 _______
_______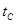 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)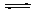 N2(g)+2CO2(g) △H<0。
N2(g)+2CO2(g) △H<0。 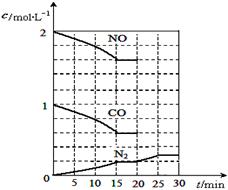
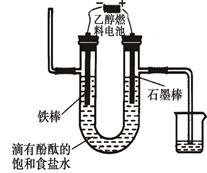
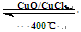 2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol
2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol 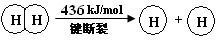

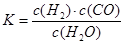 ,它所对应的化学方程式为:
,它所对应的化学方程式为:  2NH3(g) △H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分)
2NH3(g) △H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分)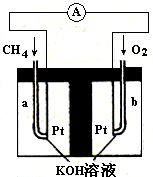


 mol;
mol;

 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)