题目内容
(I)下图是工业生产硝酸铵的流程。
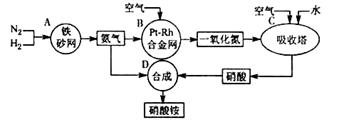
(1)吸收塔C中通入空气的目的是 。A、B、C、D四个容器中的反应,属于氧化还原反应的是 (填字母)。
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) +6H2O(g) △H =-1266.8kJ/mol
N2(g) + O2(g) = 2NO(g) △H =" +180.5" kJ/mol
写出氨高温催化氧化的热化学方程式:
(II)某合作小组同学将铜片加入稀硝酸,发现开始时反应非常慢,一段时间后反应速率明显加快。该小组通过实验探究其原因。
(3)该反应的离子方程式为___________________________________________________。
(4)提出合理假设。该实验中反应速率明显加快的原因可能是_____________________。
A.反应放热导致温度升高 B.压强增大
C.生成物有催化作用 D.反应物接触面积增大
(5)初步探究。测定反应过程中溶液不同时间的温度,结果如下表:
结合实验目的和表中数据,你得出的结论是__________________________________。
(6)进一步探究。查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用,请完成以下实验设计表并将实验目的补充完整:

(1)吸收塔C中通入空气的目的是 。A、B、C、D四个容器中的反应,属于氧化还原反应的是 (填字母)。
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) +6H2O(g) △H =-1266.8kJ/mol
N2(g) + O2(g) = 2NO(g) △H =" +180.5" kJ/mol
写出氨高温催化氧化的热化学方程式:
(II)某合作小组同学将铜片加入稀硝酸,发现开始时反应非常慢,一段时间后反应速率明显加快。该小组通过实验探究其原因。
(3)该反应的离子方程式为___________________________________________________。
(4)提出合理假设。该实验中反应速率明显加快的原因可能是_____________________。
A.反应放热导致温度升高 B.压强增大
C.生成物有催化作用 D.反应物接触面积增大
(5)初步探究。测定反应过程中溶液不同时间的温度,结果如下表:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
结合实验目的和表中数据,你得出的结论是__________________________________。
(6)进一步探究。查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用,请完成以下实验设计表并将实验目的补充完整:
| 实验 编号 | 铜片 质量/g | 0.1mol·L-1的 硝酸体积/mL | 硝酸铜 晶体/g | 亚硝酸钠 晶体/g | 实验目的 |
| ① | 5 | 20 | _______ | _______ | 实验①和②探究_________的影响;实验①和③探究亚硝酸根的影响。 |
| ② | 5 | 20 | 0.5 | 0 | |
| ③ | 5 | 20 | 0 | 0.5 |
(I)(1)使NO全部转化成HNO3 (或提供O2氧化NO)(2分); ABC(2分)(少1个扣1分,多1个没有分)
(2)4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905.8kJ/mol(3分)
4NO(g)+6H2O(g) △H=-905.8kJ/mol(3分)
(II)(3)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O (3分)
(4)AC(2分)
(5)温度不是反应速率明显加快的主要原因。(2分)
(6)(2分)
(2)4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H=-905.8kJ/mol(3分)
4NO(g)+6H2O(g) △H=-905.8kJ/mol(3分)(II)(3)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O (3分)
(4)AC(2分)
(5)温度不是反应速率明显加快的主要原因。(2分)
(6)(2分)
| 实验编号 | 铜片 质量/g | 0.1mol·L-1的 硝酸体积/mL | 硝酸铜 晶体/g | 亚硝酸钠 晶体/g | 实验目的 |
| ① | 5 | 20 | 0 | 0 | 实验①和②探究 Cu2+ 的影响;实验①和③探究亚硝酸根的影响。 |
| ② | 5 | 20 | 0.5 | 0 | |
| ③ | 5 | 20 | 0 | 0.5 |
试题分析:(1)在整个生产流程中,第一次通入空气为了提高氨气的转化率,第二次是为了提高一氧化氮生成硝酸的转化率;整个流程中涉及的反应方程式有:①N2+3H2?2NH3②4NH3+5O2 =4NO+6H2O③2NO+O2═2NO2④3NO2+H2O═2HNO3+NO
⑤4NO2+O2+H2O═4HNO3⑥NH3+HNO3═NH4NO3,其中①②③④⑤属于氧化还原反应,即ABC属于氧化还原反应。
(2)氨高温催化氧化的热化学方程式可由①+2×②可得4NH3(g)+5O2(g)= 4NO(g)+6H2O(g),所以△H=-1266.8kJ/mol+2×180.5 kJ/mol=-905.8kJ/mol
(3)铜与稀硝酸反应的离子方程式:3Cu+8H++2NO3- = 3Cu2++2NO↑+4H2O
(4)影响化学反应速率的因素有压强、浓度、温度、催化剂、接触面积等,但是在铜与稀硝酸的反应中,压强不影响,硝酸的浓度随反应进行减小,铜的接触面积也减小,因此浓度、接触面积都不会加快反应速率;但是金属与酸的反应是放热反应,所以有可能是温度升高加快了反应速率,也有可能是生成物具有催化作用,生成的物质作催化剂加快了反应,故选AC。
(5)从表格中数据可知反应的80min中温度升高不多,因此温度对反应速率影响不大,不是主要因素。
(6)排除了温度因素后,探究生成物对反应的催化作用,所以生成物中或中间产物中可能有催化作用的是Cu2+ 和亚硝酸根,所以控制变量进行探究,实验①和②探究Cu2+的影响,实验①和③探究亚硝酸根的影响。

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
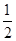 O2(g ) = CO2( g ) △H=─283.0 kJ / mol 。
O2(g ) = CO2( g ) △H=─283.0 kJ / mol 。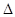 H= -Q1 kJ/mol;
H= -Q1 kJ/mol;  2NO2(g);△H=" +57.0" kJ·mol-1,NO2和N2O4的浓度如图甲所示。NO2和N2O4的消耗速率与其浓度的关系如乙图所示,
2NO2(g);△H=" +57.0" kJ·mol-1,NO2和N2O4的浓度如图甲所示。NO2和N2O4的消耗速率与其浓度的关系如乙图所示,
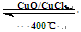 2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol
2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol 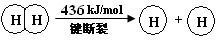

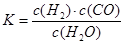 ,它所对应的化学方程式为:
,它所对应的化学方程式为:  2NH3(g) △H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分)
2NH3(g) △H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分)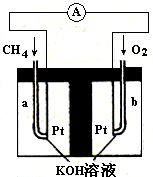
 2SO3的平衡常数见下表。
2SO3的平衡常数见下表。

 CH3OH(g) ΔH1
CH3OH(g) ΔH1
 2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。