题目内容
甲醇是一种很好的燃料,工业上可用多种原料通过不同的反应制得甲醇。
(1)已知在常温常压下:

(2)工业上正在研究利用来生产甲醇燃料的方法,该反应为:

在某温度下,将6mol CO2和8molH2充入容积为2L的密闭容器中,8分钟时达平衡状态,H2的转化率为75%。请回答:
②用CH3OH表示该反应在0-8min内的平均反应速率v(CH3OH)=____.
②此温度下该反应平衡常数K=____________ mol;
mol;
③若在上述平衡体系中,再充入2mol H2,反应达到平衡后H2的转化率____________75% (填“大于”、“小于”或“等于”)。
(3)一氧化碳与氢气也可以合成甲醇:
①若该反应在恒温恒容条件下进行,下列说法正确的是____;
a.若混合气体的密度不再改变,说明反应已达化学平衡状态
b.反应达到平衡后,通入CH3OH(g)使压强增大,平衡向右移动
c.反应达到平衡后,通入氩气使压强增大,平衡向右移动
d.反应达到平衡后,升高温度,平衡逆向移动,平衡常数减小
e.若使用催化剂,会改变反应的途径,但反应的不变
②某温度下,在一个容积为2L的密闭容器中进行该反应,已知此温度下的平衡常数K=50L2/mol2,反应到某时刻测得各组分的物质的量如下:

请比较此时正、逆反应速率的大小: (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(1)已知在常温常压下:

(2)工业上正在研究利用来生产甲醇燃料的方法,该反应为:

在某温度下,将6mol CO2和8molH2充入容积为2L的密闭容器中,8分钟时达平衡状态,H2的转化率为75%。请回答:
②用CH3OH表示该反应在0-8min内的平均反应速率v(CH3OH)=____.
②此温度下该反应平衡常数K=____________
 mol;
mol;③若在上述平衡体系中,再充入2mol H2,反应达到平衡后H2的转化率____________75% (填“大于”、“小于”或“等于”)。
(3)一氧化碳与氢气也可以合成甲醇:

①若该反应在恒温恒容条件下进行,下列说法正确的是____;
a.若混合气体的密度不再改变,说明反应已达化学平衡状态
b.反应达到平衡后,通入CH3OH(g)使压强增大,平衡向右移动
c.反应达到平衡后,通入氩气使压强增大,平衡向右移动
d.反应达到平衡后,升高温度,平衡逆向移动,平衡常数减小
e.若使用催化剂,会改变反应的途径,但反应的不变
②某温度下,在一个容积为2L的密闭容器中进行该反应,已知此温度下的平衡常数K=50L2/mol2,反应到某时刻测得各组分的物质的量如下:

请比较此时正、逆反应速率的大小:
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)(1)-1275.6 (2)① 0.125 mol/(L·min) ②0.5 ③小于 (3)① d e ② =
试题分析:(1)将①×2+②-③×4得2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)ΔH="{-442.8×2-566-(-44)" ×4}KJ/mol=-1275.6 KJ/mol.
(2)①V(H2)=ΔC(H2)/Δt={(8mol÷2L)×75%}÷8min= 0.375 mol/(L·mol); 3V(CH3OH)= V(H2),所以V(CH3OH)="1/3" V(H2)=0.375mol/(L·mol) ÷3=0.125 mol/(L·min) . ②在反应开始时C(CO2)="3mol/L," C(H2)=4mol/L,C(CH3OH)=0,C(H2O)=0.当反应达到化学平衡时,C(CO2)="2mol/L," C(H2)="1mol/L," C(CH3OH) =1mol/L,C(H2O)="1mol/L." 此温度下该反应平衡常数K="{" C(CH3OH)·C(H2O)} ÷ { C(CO2) · C(H2)}="{1×1}" ÷{2×1}=0.5.③当反应达到平衡后若再充入2mol H2,化学平衡正向移动,但平衡移动消耗的H2的物质的量远远小于投入量,所以 H2的转化率比75% 要小。即当可逆反应达到化学平衡时,加入反应物,能使其它反应物的转化率提高,但它本身的转化率反而降低。
(3)①a由于该反应是在恒温恒容条件下进行,无论反应是否达到平衡混合气体的密度不会发生改变。错误。b.反应达到平衡后,通入CH3OH(g), CH3OH(g)的浓度增大,平衡向左移动。错误。c.反应达到平衡后,通入氩气使压强增大,由于反应混合物个物质的浓度没变,所以平衡不移动。错误。d.反应达到平衡后,升高温度,化学平衡向吸热反应方向即平衡逆向移动,平衡常数减小。正确。e.若使用催化剂,会改变反应的途径,反应速率改变,但不能使化学平衡发生移动。正确。选项为:d e.
②在某时刻C(CO)=0.2mol/L,C(H2)=0.2mol/L,C(CH3OH)="0.4mol/L." C(CH3OH) ÷{ C(CO) ·C(H2)} =" 0.4mol/L" ÷(0.2mol/L×(0.2mol/L)2)= 50L2/mol2=K.所以反应达到化学平衡,此时V正=V逆

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
 2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断: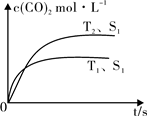
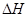 =-867kJ·mol-1
=-867kJ·mol-1 N2O4(g)
N2O4(g) 

 O2(g)=CO2(g)的 △H= kJ ? mol-1。
O2(g)=CO2(g)的 △H= kJ ? mol-1。 2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为 。
2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为 。 CH3OH(g)
CH3OH(g) 
 2SO3(g) △H="-197" kj/mol。开始时在10 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出197kJ的热量,该温度下的平衡常数K= ,升高温度K将 (填“增大、减小或不变”)。
2SO3(g) △H="-197" kj/mol。开始时在10 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出197kJ的热量,该温度下的平衡常数K= ,升高温度K将 (填“增大、减小或不变”)。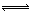 2SO3(g),化学兴趣小组的同学探究了其他条件不变时,改变某一条件时对上述反应的影响,并根据实验数据作出了下列关系图。下列判断中正确的是 (填字母)。
2SO3(g),化学兴趣小组的同学探究了其他条件不变时,改变某一条件时对上述反应的影响,并根据实验数据作出了下列关系图。下列判断中正确的是 (填字母)。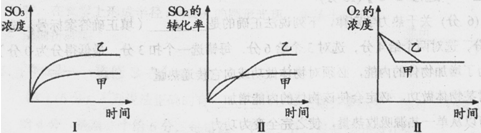
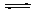 N2(g)+2CO2(g) △H<0。
N2(g)+2CO2(g) △H<0。 


 CH3OH(g),CO的平衡转化率与温度、压强的关系如下图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如下图所示,则:


 Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol
Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol 2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
 CH3COOC2H5(l)+H2O(l) ΔH=-8.62 kJ·mol-1
CH3COOC2H5(l)+H2O(l) ΔH=-8.62 kJ·mol-1