题目内容
【题目】采用湿法冶金工艺回收废旧光盘中的金属Ag(其他金属因微量忽略不计),其流程如下:
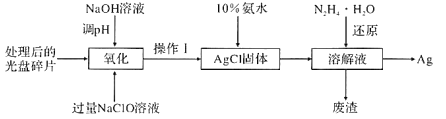
回答下列问题:
(1)①“操作I”为_____,在实验室进行此操作需要用到的玻璃仪器有_____。
②在实验室利用“操作I”的装置洗涤难溶物的操作方法是_______。
(2)若NaClO溶液与Ag反应的产物有AgCl和O2,则该反应的化学方程式为____若以稀HNO3代替NaClO溶液,其缺点是___(写出一条即可)。
(3)已知Ag2O在酸性条件下能将有毒气体甲醛(HCHO)氧化成CO2,科学家据此原理将上 述过程设计为一种电化学装置,以回收电极材料中的金属Ag。则此电池的正极反应式为_____。
(4)已知室温时,Ksp(Ag2SO4)=1.4×10-5,Ksp(AgCl)=1.8×10-10。计算反应Ag2SO4(s)+2Cl-(aq) ![]() 2AgCl(s)+SO42- (aq)的平衡常数K=_____。(保留两位有效数字)
2AgCl(s)+SO42- (aq)的平衡常数K=_____。(保留两位有效数字)
【答案】过滤 烧杯、漏斗、玻璃棒 向过滤器内加蒸馏水浸没沉淀,使水自然流下,重复 2~3 次 4Ag+ 4NaClO + 2H2O = 4AgCl + 4NaOH + O2↑ 没有 Cl-不能生成 AgCl(或生成氮氧化物,污染空气) Ag2O + 2e- + 2H+ = 2Ag + H2O 4.3×1014
【解析】
(1)①“操作I”得到溶液和固体,故为过滤;在实验室进行此操作需要用到的玻璃仪器有烧杯、漏斗、玻璃棒;
②在实验室利用“操作I”的装置洗涤难溶物的操作方法是向过滤器内加蒸馏水浸没沉淀,使水自然流下,重复 2~3 次;
(2)若NaClO溶液与Ag反应的产物有AgCl和O2,银元素和氧元素化合价升高,则氯元素化合价降低,根据氧化还原反应进行配平得反应的化学方程式为4Ag+ 4NaClO + 2H2O = 4AgCl + 4NaOH + O2↑;
若以稀HNO3代替NaClO溶液,其缺点是没有 Cl-不能生成 AgCl、生成氮氧化物,污染空气;
(3)已知Ag2O在酸性条件下能将有毒气体甲醛(HCHO)氧化成CO2,科学家据此原理将上 述过程设计为一种电化学装置,以回收电极材料中的金属Ag。则此电池的正极氧化银得电子产生银,电极反应式为Ag2O + 2e- + 2H+ = 2Ag + H2O;
(4)已知室温时,Ksp(Ag2SO4)=1.4×10-5,Ksp(AgCl)=1.8×10-10。计算反应Ag2SO4(s)+2Cl-(aq) ![]() 2AgCl(s)+ SO42- (aq)的平衡常数K=
2AgCl(s)+ SO42- (aq)的平衡常数K=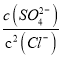 =
= =
= =
= =4.3×1014。
=4.3×1014。

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案