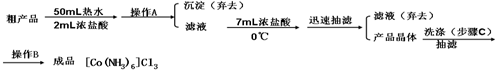
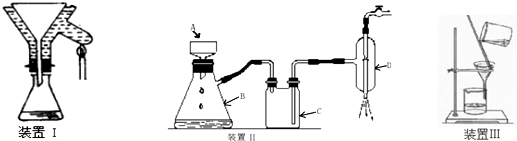
题目内容
下列说法正确的是( )
| A、电解精炼铜时,同一时间内阳极溶解铜的质量与阴极析出铜的质量相等 |
| B、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| C、过程的自发性不仅能用于判断过程的方向,还能确定过程是否一定能发生 |
| D、S(g)+O2(g)=SO2(g)△H1,S(s)+O2(g)=SO2(g)△H2;则△H1<△H2 |
考点:电解原理,反应热和焓变,化学平衡的影响因素
专题:
分析:A.阴极和阳极的电子得失守恒,阳极是不纯的铜,含有其他金属或者非金属,阳极失去的电子由铜和其他金属承担;阴极析出较纯的铜单质,电子全部由较纯的铜提供;
B.减少生成物的浓度,反应速率减小;
C.过程的自发性不能确定过程是否一定能发生;
D.固体硫燃烧时要先变为气态硫,过程吸热,据此确定反应热的大小.
B.减少生成物的浓度,反应速率减小;
C.过程的自发性不能确定过程是否一定能发生;
D.固体硫燃烧时要先变为气态硫,过程吸热,据此确定反应热的大小.
解答:
解:A.阴极和阳极的电子得失守恒,阳极是不纯的铜,含有其他金属或者非金属,阳极失去的电子由铜和其他金属承担;阴极析出较纯的铜单质,电子全部由较纯的铜提供;因此阳极溶解的铜肯定比阴极析出的纯铜质量少,故A错误;
B.减少生成物的浓度,反应速率减小,则合成氨生产过程中将NH3液化分离,减小正反应速率,平衡正移,提高N2、H2的转化率,故B错误;
C.过程的自发性仅能用于判断过程的方向,不能确定过程是否一定能发生,故C错误;
D.固体硫燃烧时要先变为气态硫,过程吸热,气体与气体反应生成气体比固体和气体反应生成气体产生热量多,但反应热为负值,所以△H1<△H2,故D正确;
故选D.
B.减少生成物的浓度,反应速率减小,则合成氨生产过程中将NH3液化分离,减小正反应速率,平衡正移,提高N2、H2的转化率,故B错误;
C.过程的自发性仅能用于判断过程的方向,不能确定过程是否一定能发生,故C错误;
D.固体硫燃烧时要先变为气态硫,过程吸热,气体与气体反应生成气体比固体和气体反应生成气体产生热量多,但反应热为负值,所以△H1<△H2,故D正确;
故选D.
点评:本题综合考查学生电化学、热化学、化学反应的自发性以及反应速率等方面的知识,属于综合知识的考查,难度中等.

练习册系列答案
相关题目
对于重水D2O,在25℃时KW=10-12,定义pD=-lg{c(D+)},pOD=-lg{c(OD-)}.则下列说法正确的是( )
| A、25℃时,纯重水pD=7 |
| B、25℃时,0.1mol/L NaCl的重水溶液pD=pOD=6 |
| C、25℃时,1mol/L的DCl的重水溶液pD=0,pOD=14 |
| D、25℃时,0.01mol/L NaOD的重水溶液中pD=12 |
下列离子方程式正确的是( )
| A、三氯化铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ |
| B、向含有0.2 mol FeI2的溶液中通入0.25 mol Cl2:8I-+2Fe2++5Cl2═10Cl-+4I2+2Fe3+ |
| C、K37ClO3与浓盐酸(HCl)在加热时生成Cl2:37ClO3-+6HCl═37Cl-+3Cl2↑+3H2O |
| D、将0.1 mol/L盐酸数滴缓缓滴入0.1 mol/L 25 mL Na2CO3溶液中,并不断搅拌:2H++CO32-═CO2↑+H2O |
苹果酸的结构简式为 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、苹果酸中能发生酯化反应的官能团有2种 |
| B、1 mol苹果酸可与3 mol NaOH发生中和反应 |
| C、1 mol苹果酸与足量金属Na反应生成1 mol H2 |
D、 与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
已知在中性条件下钢铁易发生吸氧腐蚀时,正极上发生的电极反应是( )
| A、2H++2e-→H2 |
| B、Fe2++3e→Fe |
| C、2H2O+O2+4e-→4OH- |
| D、Fe3+-e→Fe3+ |