题目内容
FeSO4摩尔质量 ; Al2(SO4)3摩尔质量 ; HNO3摩尔质量 ;
HCl摩尔质量 ; Fe3+摩尔质量 ; SO42-摩尔质量 .
HCl摩尔质量
考点:摩尔质量
专题:
分析:一种物质的摩尔质量在数值上等于该物质的相对分子质量或相对原子质量,单位为g/mol.
解答:
解:FeSO4的相对分子质量为152,摩尔质量为152g/mol;
Al2(SO4)3的相对分子质量为342,摩尔质量为342g/mol;
HNO3的相对分子质量为63,摩尔质量为63g/mol;
HCl的相对分子质量为36.5,摩尔质量为36.5g/mol;
Fe3+的相对分子质量为56,摩尔质量为56g/mol;
SO42-的相对分子质量为96,摩尔质量为96g/mol;
故答案为:152g/mol;342g/mol;63g/mol;36.5g/mol;56g/mol;96g/mol.
Al2(SO4)3的相对分子质量为342,摩尔质量为342g/mol;
HNO3的相对分子质量为63,摩尔质量为63g/mol;
HCl的相对分子质量为36.5,摩尔质量为36.5g/mol;
Fe3+的相对分子质量为56,摩尔质量为56g/mol;
SO42-的相对分子质量为96,摩尔质量为96g/mol;
故答案为:152g/mol;342g/mol;63g/mol;36.5g/mol;56g/mol;96g/mol.
点评:根据一种物质的摩尔质量在数值上等于该物质的相对分子质量或相对原子质量,单位为g/mol,难度不大.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
下列事实,不能用平衡移动原理解释的是( )
| A、硫酸工业中,增大O2的浓度有利于提高SO2的转化率 |
| B、将FeS固体投入到含有Cu2+的废水中以除去Cu2+ |
| C、选择合适的催化剂可使水在较低温度下分解 |
| D、滴有酚酞的CH3COONa溶液,加热后颜色变深 |
下列说法正确的是( )
| A、1molO2所占体积约为22.4L |
| B、22gCO2中含有的原子数约为6.02×1023 |
| C、100mL0.5mol/LKCl溶液中含溶质的质量为0.05g |
| D、标准状况下,11.2LN2和H2的混合气体所含分子数约为3.01×1023 |
下列说法正确的是( )
| A、只有在原子中,质子数才与核外电子数相等 |
| B、O2-半径比F-的小 |
| C、Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 |
| D、P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的弱 |
下列各项内容中,排列顺序正确的是( )
| A、固体的热稳定性:Na2CO3>CaCO3>NaHCO3 |
| B、金属活动性Li>Na>K |
| C、氧化物的稳定性:H2Se>H2S |
| D、微粒半径:K+>S2->F- |
某些化学概念在逻辑上存在下图所示关系,则下列说法中正确的是:( )

| A、纯净物(B)与混合物(A)属于包含关系 |
| B、化合物(B)与氧化物(A)属于包含关系 |
| C、单质与化合物属于交叉关系 |
| D、氧化反应与化合反应属于并列关系 |
下列说法正确的是( )
| A、16O2与18O2互为同位素,H2O、D2O、T2O互为同素异形体,N60和N2互为同系物 |
| B、除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| C、非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价 |
D、Ca的原子结构示意图为 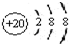 |
1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献.他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化.下列说法正确的是( )
| A、化学不做实验,就什么都不知道 |
| B、化学不再需要实验 |
| C、化学不再是纯实验科学 |
| D、未化学的方向是经验化 |
下列说法正确的是( )
| A、电解精炼铜时,同一时间内阳极溶解铜的质量与阴极析出铜的质量相等 |
| B、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| C、过程的自发性不仅能用于判断过程的方向,还能确定过程是否一定能发生 |
| D、S(g)+O2(g)=SO2(g)△H1,S(s)+O2(g)=SO2(g)△H2;则△H1<△H2 |