题目内容
16.若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是( )| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、Mg2+、HCO3- | ||
| C. | NO3-、Cl-、Fe2+、K+ | D. | NO3-、AlO2-、OH-、K+ |
分析 加入铝粉能放出氢气的溶液,为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:加入铝粉能放出氢气的溶液,为非氧化性酸或强碱溶液,
A.酸性溶液中不能大量存在CO32-,碱性溶液中不能大量存在NH4+,故A不选;
C.酸性溶液中不能大量存在HCO3-,碱性溶液中不能大量存在Mg2+、HCO3-,故B不选;
C.酸性溶液中NO3-、Fe2+、H+发生氧化还原反应,碱性溶液中不能大量存在Fe2+,故C不选;
D.碱性溶液中该组离子之间不反应,可大量共存,故D选;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
相关题目
4.下列转化必须加入还原剂才能实现的是( )
| A. | Fe3+→Fe2+ | B. | Zn→Zn2+ | C. | H2→H2O | D. | Cl2→Cl- |
8.已知常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol•L-1.(已知H2CO3的第二级电离常数K2=5.6×10-11,HClO的电离常数K=3.0×10-8,已知10-5.60=2.5×10-6).下列选项中不正确的是( )
| A. | 若忽略水的电离及H2CO3的第二级电离,则H2CO3?HCO3-+H+的平衡常数K1=4.2×10-7 | |
| B. | 少量Cl2通入到过量的Na2CO3溶液的离子方程式为Cl2+2CO32-+H2O═2HCO3-+Cl-+ClO- | |
| C. | Cl2与Na2CO3按物质的量之比1:1恰好反应的离子方程式为Cl2+CO32-+H2O═HCO3-+Cl-+HClO | |
| D. | 少量CO2通入到过量的NaClO溶液的离子方程式为2ClO-+CO2+H2O═CO32-+2HClO |
5.甲、乙两同学用一种标准盐酸去测定同一种未知浓度的NaOH溶液的浓度,但操作不同;甲把一定体积的NaOH溶液放入锥形瓶,把标准盐酸放入滴定管进行滴定;乙把一定体积的标准盐酸放入锥形瓶,把未知液NaOH溶液放入滴定管进行滴定.
(1)甲同学使用的是酸式滴定管,乙同学使用的是碱式滴定管.
(2)甲同学的滴定管在用蒸馏水洗净后没有用标准盐酸润洗,乙同学的滴定管在用蒸馏水洗净后也没有用待测NaOH 溶液润洗,其余操作均正确,这样甲同学测定结果偏大(偏大、偏小、无影响,下同),乙同学测定结果偏小.
(3)乙同学选择酚酞作指示剂进行试验,如何来判断滴定终点:滴入最后一滴NaOH溶液,锥形瓶中溶液由无色变为粉红色,且30秒内不褪色
(4)甲同学根据三次实验分别记录有关数据如表:
请选用其中合理的数据计算c(NaOH)=0.1044mol/L.
(1)甲同学使用的是酸式滴定管,乙同学使用的是碱式滴定管.
(2)甲同学的滴定管在用蒸馏水洗净后没有用标准盐酸润洗,乙同学的滴定管在用蒸馏水洗净后也没有用待测NaOH 溶液润洗,其余操作均正确,这样甲同学测定结果偏大(偏大、偏小、无影响,下同),乙同学测定结果偏小.
(3)乙同学选择酚酞作指示剂进行试验,如何来判断滴定终点:滴入最后一滴NaOH溶液,锥形瓶中溶液由无色变为粉红色,且30秒内不褪色
(4)甲同学根据三次实验分别记录有关数据如表:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
6..在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是( )
| A. | 两种气体的物质的量相等 | B. | O2比O3的质量小 | ||
| C. | 两种气体的分子数目相等 | D. | 两种气体中的氧原子数目相等 |
 ;
;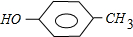 和
和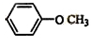 .
.