题目内容
1.A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
(1)常温下含碳量最高的气态烃是D(填字母).
(2)能够发生加成反应的烃有4种.
(3)上述有机物的一卤代物种类最多的是甲苯(填名称).
(4)①写出实验室制C的化学方程式CH3CH2OH$→_{△}^{浓硫酸}$CH2=CH2↑+H2O.
②上述化学反应的类型是c
a.加成 b.取代 c.消去 d.氧化
③若将反应物改成一种卤代烃和某种溶液的混合物,也有C的生成,请写出这个反应的化学方程式:CH3CH2Cl+NaOH$→_{△}^{醇}$CH2=CH2↑+NaCl+H2O
(5)写出F发生硝化反应的化学方程式
 +HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$
+HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.
分析 由结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,根据物质的组成、结构和性质解答该题.
解答 解:由结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,
(1)常温下含碳量最高的气态烃是乙炔,故答案为:D;
(2)能够发生加成的烃有有乙烯、乙炔、苯和甲苯4种,故答案为:4;
(3)一卤代物种类最多的是甲苯,共有4种,故答案为:甲苯;
(4)C为乙烯,实验室用乙醇和浓硫酸发生消去反应制备,反应的方程式为CH3CH2OH$→_{△}^{浓硫酸}$CH2=CH2↑+H2O,若将反应物改成一种卤代烃和某种溶液的混合物,也有C的生成,这个反应的化学方程式为CH3CH2Cl+NaOH$→_{△}^{醇}$CH2=CH2↑+NaCl+H2O,
故答案为:CH3CH2OH$→_{△}^{浓硫酸}$CH2=CH2↑+H2O;c;CH3CH2Cl+NaOH$→_{△}^{醇}$CH2=CH2↑+NaCl+H2O;
(5)F为苯,可与浓硝酸在浓硫酸作用下加热制备三硝基苯,反应的方程式为 +HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$
+HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$ +H2O,
+H2O,
故答案为: +HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$
+HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.将铜丝插入浓硫硫加热取出后,在铜丝表面会产生一层黑色固体甲,为研究固体甲的成分,进行下实验.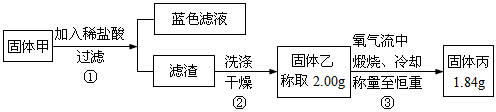
已知,氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,Cu在氧气流中锻烧,可以转化为氧化铜.硫化铜和硫化亚铜常温下都不溶于稀盐,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫.
下列用关说法正确的是( )

已知,氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,Cu在氧气流中锻烧,可以转化为氧化铜.硫化铜和硫化亚铜常温下都不溶于稀盐,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫.
下列用关说法正确的是( )
| A. | 加盐酸有蓝色溶液生成,说明固体甲中一定含有氧化铜 | |
| B. | 步骤①所得滤渣中肯定含有单质铜 | |
| C. | 固体甲中若存在Cu2O,也可能有Cu2S | |
| D. | 固体甲中,CuS和Cu2S不能同时存在 |
9.在核反应方程24He+714N→817O+X中,X代表的粒子是( )
| A. | 11H | B. | 12H | C. | -10e | D. | 01n |
16.等质量的Na、Mg、Al三种金属与足量稀硫酸反应,在标准状况下生成的氢气由多到少的顺序是( )
| A. | Na>Mg>Al | B. | Al>Mg>Na | C. | Mg>Al>Na | D. | Na>Al>Mg |
6.质量为a g的铜丝放在空气中灼烧变黑,趁热放入下列物质中,铜丝变红,质量仍为a g的是( )
| A. | CH3COOH | B. | HNO3 | C. | CH3CH2OH | D. | NaOH |