题目内容
13.向50mL 0.018mol/L 的AgNO3溶液中,加入50mL 0.02mol/L 的盐酸,生成了沉淀.如果溶液中c(Ag+)、c(Cl-)的乘积是一个常数:c(Ag+)•c(Cl-)=1.0×10-10,求:①沉淀生成后溶液中c(Ag+)是多少?
②反应后溶液的pH 是多少?
分析 ①结合n=cV计算离子的物质的量,判断过量,由沉淀后溶液中氯离子浓度、结合Ksp计算溶液中银离子浓度;
②沉淀前后溶液中氢离子物质的量不变,由混合后氢离子的浓度计算pH.
解答 解:①向50mL 0.018mol/L的AgNO3溶液中加入50mL 0.02mol/L的盐酸,混合后两者浓度分别为c(Ag+)=$\frac{0.05L×0.018mol/L}{0.1L}$=0.009 mol/L、c(Cl-)=$\frac{0.05L×0.02mol/L}{0.1L}$=0.01mol/L,Ag+与Cl-是等物质的量反应的,此时Cl-过量,过量浓度c(Cl-)=0.01-0.009=0.001mol/L,
Ksp=c(Ag+)×C(Cl-)=1.0×10-10,则:c(Ag+)=$\frac{1.0×1{0}^{-10}}{0.001}$=1.0×10-7mol/L,
答:沉淀生成后溶液中c(Ag+)是1.0×10-7mol/L;
②沉淀生成后,氢离子浓度为$\frac{0.05L×0.02mol/L}{0.1L}$=0.01mol/L,所以pH=-lg10-2=2,
答:沉淀生成后溶液的pH是2.
点评 本题考查难溶电解质的生成及Ksp计算,为高频考点,把握过量判断、Ksp计算为解答的关键,侧重分析与计算能力的考查,注意等体积混合后离子浓度变化,题目难度不大.

练习册系列答案
相关题目
18.中华民族的发明创造为人类文明进步做出了巨大贡献.下列我国古代发明中,不涉及化学反应的是( )
| A. |  打磨磁石制指南针 | B. |  烧结粘土制陶瓷 | ||
| C. |  湿法炼铜 | D. |  铁的冶炼 |
2.下列说法正确的是( )
| A. | 将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入足量NH3,产生沉淀 | |
| B. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| C. | 盛放氢氧化钠溶液的试剂瓶用橡皮塞,不用玻璃塞 | |
| D. | Na2O2与水反应、红热的Fe与水蒸气反应均能生成碱 |
3.在密闭容中发生下列反应aA(g)?cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述不正确的是( )
| A. | A的转化率变小 | B. | 平衡向逆反应方向移动 | ||
| C. | D的质量百分数变大 | D. | a<c+d |

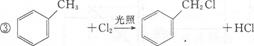
 +HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$
+HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.
 是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
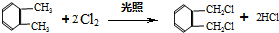 .
.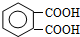 +2CH3CH2OH
+2CH3CH2OH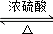
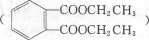 +2H2O.
+2H2O.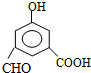 ,每种同分异构体中,化学环境不同的氢原子都是6种.
,每种同分异构体中,化学环境不同的氢原子都是6种.