题目内容
14.期元素X、Y、Z、W的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y 的次外层电子数是最外层的$\frac{1}{3}$,Z被称为“国防金属”,W与Y属于同一主族.下列叙述正确的是( )| A. | 原子半径:W>Z>Y | |
| B. | Y形成的离子与Z形成的离子的电子数可能相同 | |
| C. | 化合物ZY、WY3 中化学键的类型相同 | |
| D. | 由X、Y、Z、W组成的化合物的水溶液不可能显酸性 |
分析 短周期元素X、Y、Z、W的原子序数依次增大,X的原子在元素周期表中原子半径最小,则X为H元素;Y的次外层电子数是最外层的$\frac{1}{3}$,Y原子只能有2个电子层,最外层电子数为6,则Y为O元素;W与Y属于同一主族,则W为S元素;Z被称为“国防金属”,则Z为Mg,以此解答该题.
解答 解:根据分析得出X为H元素;Y为O元素;W为S元素;Z为Mg元素,
A.原子半径最小的原子X为H,同周期随原子序数增大原子半径减小,故原子半径Mg>S>O,即Z>W>Y,故A错误;
B.Y形成的离子有O2-、O22-,其中O22-与Z形成的离子S2-电子数都是18,故B正确;
C.ZY是MgO,MgO中为离子键,WY3是SO3,SO3中为共价键,故C错误;
D.X、Y、Z、W可组成化合物MgSO4•7H2O,其中Mg2+水解显酸性,故D错误;
故选:B.
点评 本题考查结构位置性质关系应用、元素周期律、化学键、盐类水解等,为高频考点,侧重于学生的分析能力的考查,难度中等,推断元素是解题关键.

练习册系列答案
相关题目
14.从安全的角度,下列做法正确的是( )
| A. | 水银温度计不慎被打破,用胶头滴管将水银吸出放入水封的瓶中,残破的温度计插入装有硫粉在广口瓶中 | |
| B. | 用氢气还原氧化铜的实验中,开始应该先点燃酒精灯后通氢气 | |
| C. | 遇到氯气泄漏时,应立即关闭氯气罐,用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处 | |
| D. | 乘坐火车时,严禁携带白磷、汽油、氯化钠等易燃易爆物品 |
19.下列由实验操作和实验现象能得出实验结论或推论的是( )
| 实验操作 | 实验现象 | 结论或推论 | |
| A | 溴水中加入甲苯,振荡 | 水层几乎呈无色 | 甲苯与溴发生了反应 |
| B | 一小粒金属钠投入无水乙醇中 | 最后钠浮在液面上 | 密度:乙醇大于钠 |
| C | Fe(SCN)3溶液中滴入足量NaOH溶液 | 澄清后得到无色溶液 | Fe(OH)3悬浊液中滴加KSCN溶液后不显红色 |
| D | 在含Mn2+的草酸溶液中滴加酸性高锰酸钾溶液 | 高锰酸钾溶液褪色较快 | 反应过程中,Mn2+一定氧化了草酸 |
| A. | A | B. | B | C. | C | D. | D |
6.制乙烯时,还产生少量SO2、CO2及水蒸气,某研究小组用下列装置检验这四种气体,仪器连接顺序正确的是( )
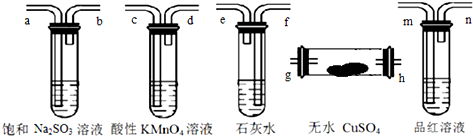

| A. | h-g-m-n-a-b-f-e-c-d | B. | g-h-m-n-a-b-e-f-c-d | ||
| C. | h-g-c-d-m-n-f-e-a-b | D. | h-g-m-n-c-d-e-f-a-b |
3.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 30 g乙烷中所含的极性共价键数为7NA | |
| B. | 常温常压下,28g乙烯与丁烯的混合气体含有的碳原子数目NA | |
| C. | 密闭容器中2molNO与1molO2充分反应,产物的分子数小于2NA | |
| D. | 标准状况下,22.4L HF含有的分子数目为NA |
4.2016年5月26日在上海举办的“食品安全和科技大会”旨在研讨食品安全问题.下列做法正确的是( )
| A. | 水果表面喷洒驱虫剂不招苍蝇 | B. | 自来水使用氯制剂以杀菌消毒 | ||
| C. | 牛肚用甲醛浸泡使其口感更好 | D. | 生豆芽时用植物生长激素提高产量 |
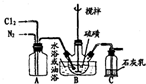 黄红色液体二氯化二硫可以作为贵稀金属的萃取剂,是由硫与氯气在50~60℃直接化合而成.装置图如下:
黄红色液体二氯化二硫可以作为贵稀金属的萃取剂,是由硫与氯气在50~60℃直接化合而成.装置图如下: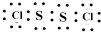 .
.
 .
. CH2OCH2CH2CHO
CH2OCH2CH2CHO =CHCH2CH2CHCHO
=CHCH2CH2CHCHO COOCH2CH2CH3
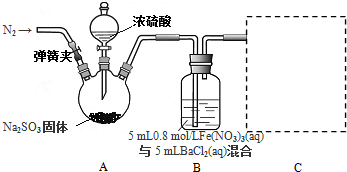
COOCH2CH2CH3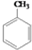 到D的合成路线(无机试剂任选,用合成路线流程图表示).
到D的合成路线(无机试剂任选,用合成路线流程图表示).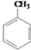 →
→