题目内容
18.三种卤化铅的溶解度曲线如图所示,下列说法正确的是( )
| A. | 三种卤化铅的溶解度均随温度的升高而减小 | |
| B. | 20℃时,PbCl2的Ksp约为1.87×10-4 | |
| C. | 任何温度下,始终存在:Ksp(PbCl2>Ksp(PbBr2>Ksp(PbI2) | |
| D. | 常温下,向浓度均为0.1mol•L-1的Cl-、Br-、I-混合溶液中,逐滴加入的Pb(NO3)2溶液,PbCl2最先沉淀 |
分析 A.依据图中三种卤化铅的溶解度曲线图解答;
B.计算20℃时,PbCl2的饱和溶液中Pb2+的物质的量浓度,氯离子浓度,依据溶度积表达式计算;
C.依据图中三种卤化铅的溶解度曲线图判断;
D.依据图中三种卤化铅的溶解度曲线可知,相同温度下,碘化铅溶解度最小,向浓度均为0.1mol•L-1的Cl-、Br-、I-混合溶液中,碘化铅先达到溶度积常数;
解答 解:A.依据图中三种卤化铅的溶解度曲线图可知:三种卤化铅的溶解度均随温度的升高而增大,故A错误;
B.1g氯化铅的物质的量为$\frac{1g}{278g/mol}$=0.0036mol;100g溶液体积约为0.1L,则铅离子的物质的量浓度为:
$\frac{0.0036mol}{0.1L}$=0.036mol/L,氯离子物质的量浓度为0.036mol/L×2=0.072mol/L,则PbCl2的Ksp约为:
C(Pb2+)C2(Cl-)=0.036mol/L×0.072mol/L×0.072mol/L=1.87×10-4(mol/L)3,故B正确;
C.依据图中三种卤化铅的溶解度曲线图,当温度小于35度时,相同温度下氯化铅溶解度大于溴化铅,当温度高于35度时,相同温度下,溴化铅溶解度大于氯化铅,故C错误;
D.依据图中三种卤化铅的溶解度曲线可知,相同温度下,碘化铅溶解度最小,向浓度均为0.1mol•L-1的Cl-、Br-、I-混合溶液中,碘化铅先达到溶度积常数,所以碘化铅最先析出,故D错误;
故选:B.
点评 本题考查了物质的溶解度,准确把握三种卤化铅的溶解度曲线是解题关键,注意溶度积规则的应用,题目难度中等.

练习册系列答案
相关题目
9.下列分子中所有原子都满足最外层为8电子结构的是( )
| A. | CCl4 | B. | HClO | C. | PCl5 | D. | NH3 |
6.某烃的结构简式为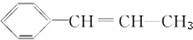 ,它可能具有的性质是( )
,它可能具有的性质是( )
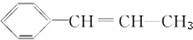 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水也易溶于有机溶剂 | |
| B. | 能发生加聚反应,其生成物可用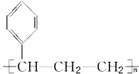 表示 表示 | |
| C. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 | |
| D. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 |
13.运用元素周期律分析下面的推断,其中不正确的是( )
| A. | 硒化氢(H2Se)是有色、有毒的气体,比H2S稳定 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| D. | 硫酸锶(SrSO4)是难溶于水的白色固体 |
3.下列有机物中,能在一定条件下发生消去反应且生成的烯烃只有一种的是( )
| A. | 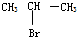 | B. | 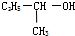 | C. | CH3OH | D. | 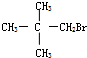 |
10.已知短周期元素的离子 aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径:B>A>C>D | B. | 原子序数:d>c>b>a | ||
| C. | 离子半径:D ->C 2->B +>A 2+ | D. | 离子的还原性:D ->C 2- |
7.硝酸在反应中只表现强氧化性的反应是( )
| A. | C与浓HNO3反应 | B. | Cu与浓HNO3反应 | C. | Cu与稀HNO3反应 | D. | Mg(OH)2与HNO3反应 |