题目内容
有同温、同压、同体积的两份气体样品,一份是CO,另一份是CO2,这两份气体样品中,CO和CO2所含氧原子的个数比是( )
| A、1:2 | B、2:1 |
| C、1:1 | D、1:4 |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:同温同压下,气体摩尔体积相等,相同体积的不同气体其物质的量相等、分子数相等,再结合分子的构成来确定氧原子个数.
解答:
解:同温同压下,气体摩尔体积相等,相同体积的不同气体其物质的量相等、分子数相等,一个CO分子中含有一个O原子、一个二氧化碳分子中含有两个O原子,所以CO和CO2所含氧原子的个数比为1:2,
故选A.
故选A.
点评:本题考查了阿伏伽德罗定律及其推论,明确气体摩尔体积的适用范围及条件是解本题关键,灵活运用基本公式结合分子构成来分析解答,题目难度不大.

练习册系列答案
相关题目
下列4种化合物从化学性质上看,有1种与其他3种明显不同,这种物质是( )
| A、CaO |
| B、SO3 |
| C、CuO |
| D、K2O |
某研究性学习小组的同学做了一个趣味实验:将一只鸡蛋放入食醋中,过一会发现蛋壳表面附有气泡,第二天蛋壳就变软了.你认为鸡蛋壳与食醋发生反应的离子方程式正确的是( )
| A、CO32-+2H+→H2O+CO2↑ |
| B、CaCO3+2H+→Ca2++H2O+CO2↑ |
| C、CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
| D、CO32-+2CH3COOH→2CH3COO-+H2O+CO2↑ |
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、5.6g铁与足量的盐酸反应转移的电子数为0.3NA |
| B、常温常压下,11.2L甲烷中含有的氢原子数为2NA |
| C、标准状况下,22.4L氦气与22.4L氟气所含原子数均为2NA |
| D、常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA |
下列各装置中,能够成原电池的是( )
A、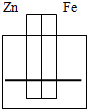 乙醇 |
B、 稀硫酸 |
C、 稀硫酸 |
D、 稀硫酸 稀硫酸 |
设nA为阿伏加德罗常数的值,下列说法正确的是( )
| A、28g N2含有的原子数为NA |
| B、标准状况下22.4L水中含有的H2O分子数为NA |
| C、1mol Zn与足量盐酸反应失去的电子数为2NA |
| D、0.1L 2mol/L NaCl溶液中含有Na+个数为2NA |
下列各组物质互为同分异构体的是( )
| A、乙醇和丙醇 |
| B、淀粉与纤维素 |
C、 |
D、CH3CH2CH2CH2CH3与 |
 ,比较它们的电子层数和核电荷数,按照Na、Mg、Al顺序排布,试解释它们金属性逐渐减弱的原因.
,比较它们的电子层数和核电荷数,按照Na、Mg、Al顺序排布,试解释它们金属性逐渐减弱的原因.