题目内容
amol由乙烯和乙烷组成的混合气体与bmol氧气于某密闭容器中,点燃充分燃烧后,乙烯与乙烷已经全部消耗完,得到一氧化碳与二氧化碳的混合气体和45g水,则:
(1)当a=1时,且反应后CO和CO2混合气体的物质的量为反应前氧气的
时,则b= ,得到的CO和CO2的物质的量之比n(CO):n(CO2)= .
(2)a取值范围是(以分数表示) ;b取值范围是(含a的式子) .
(1)当a=1时,且反应后CO和CO2混合气体的物质的量为反应前氧气的
| 2 |
| 3 |
(2)a取值范围是(以分数表示)
考点:有关混合物反应的计算
专题:烃及其衍生物的燃烧规律
分析:(1)根据碳元素守恒计算反应后CO和CO2混合气体的物质的量之和,据此计算b的值;
设反应后CO和CO2的物质的量分别为amol、bmol,根据二者之和与氧原子守恒列方程计算;
(2)根据H原子守恒利用极限法解答,只有乙烯时,a值最大,只有乙烷时,a值最小;
amol混合烃中含有2amolC,燃烧产物是一氧化碳和二氧化碳的混合物来计算b的取值范围.
设反应后CO和CO2的物质的量分别为amol、bmol,根据二者之和与氧原子守恒列方程计算;
(2)根据H原子守恒利用极限法解答,只有乙烯时,a值最大,只有乙烷时,a值最小;
amol混合烃中含有2amolC,燃烧产物是一氧化碳和二氧化碳的混合物来计算b的取值范围.
解答:
解:(1)根据碳元素守恒可知,反应后CO和CO2混合气体的物质的量之和为1mol×2=2mol,
则:
bmol=2mol,
解得:b=3;
45g水的物质的量为:
=
mol=
mol,设反应后CO和CO2的物质的量分别为xmol、ymol,
根据二者之和与氧原子守恒列方程,则:x+y=2,x+2y=3×2-
,
解得:a=0.5,b=1.5,
则:n(CO):n(CO2)=0.5mol:1.5mol=1:3,
故答案为:3;1:3;
(2)生成水的物质的量=
=2.5mol只有乙烯时,a值最大,根据H原子守恒可知,a的极大值为
=
mol,只有乙烷时,a值最小,根据H原子守恒可知,a的极小值为
=
mol,故a的取值范围是:
<a<
,
如果2.5mol水中含有2.5mol氧原子,生成2.5mol水需要消耗氧气的物质的量为:2.5mol×
=
mol,
当amol乙烯和乙烷中含有2a molC原子,若碳原子完全转化成二氧化碳,消耗的氧气的量最大,最大量为:2a mol+
mol;
当2amolC完全转化成CO时,消耗氧气的物质的量最小,则b的最小值为:amol+
mol,
因此b的取值范围是:a+
<b<2a+
,
故答案为:
<a<
;a+
<b<2a+
.
则:
| 2 |
| 3 |
解得:b=3;
45g水的物质的量为:
| 45g |
| 18g/mol |
| 45 |
| 18 |
| 5 |
| 2 |
根据二者之和与氧原子守恒列方程,则:x+y=2,x+2y=3×2-
| 5 |
| 2 |
解得:a=0.5,b=1.5,
则:n(CO):n(CO2)=0.5mol:1.5mol=1:3,
故答案为:3;1:3;
(2)生成水的物质的量=
| 45g |
| 18g/mol |
| 2.5mol×2 |
| 4 |
| 5 |
| 4 |
| 2.5mol×2 |
| 6 |
| 5 |
| 6 |
| 5 |
| 6 |
| 5 |
| 4 |
如果2.5mol水中含有2.5mol氧原子,生成2.5mol水需要消耗氧气的物质的量为:2.5mol×
| 1 |
| 2 |
| 5 |
| 4 |
当amol乙烯和乙烷中含有2a molC原子,若碳原子完全转化成二氧化碳,消耗的氧气的量最大,最大量为:2a mol+
| 5 |
| 4 |
当2amolC完全转化成CO时,消耗氧气的物质的量最小,则b的最小值为:amol+
| 5 |
| 4 |
因此b的取值范围是:a+
| 5 |
| 4 |
| 5 |
| 4 |
故答案为:
| 5 |
| 6 |
| 5 |
| 4 |
| 5 |
| 4 |
| 5 |
| 4 |
点评:本题考查了混合物的有关计算,题目难度中等,注意掌握利用原子守恒进行化学计算的方法,(2)中计算消耗氧气的物质的量b的范围为难点、易错点,注意明确解答方法.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
在一定条件下,将2mol A和1mol B混合于固定容积为2L的密闭容器中,发生如下反应:
,5s时测得气体压强是反应前的
,此段时间内C的平均生成率为( )
| 3A(g)+B(g) |
| xC(g)+2D(g) |
| 5 |
| 6 |
| A、0.25mol/L/s |
| B、0.1 |
| C、0.05mol/(L?s) |
| D、条件不足,无法计算 |
向200mL1.5mol?L-1的硫酸溶液中加入一定量Fe2O3、Cu的混合物,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,剩余固体的质量为( )
| A、17.6g | B、22.4g |
| C、2.4g | D、4.8g |
下列化学实验事实及其结论正确的是( )
| A、向碘水中滴加CCl4,振荡后静置,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
| B、Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| C、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| D、高温下,用金属钠与氯化钾可以置换出金属钾,说明钠的金属性比钾强 |
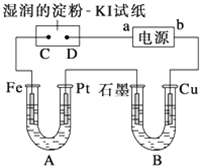 电解装置如图所示.图中B装置盛1L2mol?L-1的Na2SO4溶液,A装置中盛1L2mol?L-1 AgNO3溶液.通电后,湿润的淀粉KI试纸的C端变蓝色.电解一段时间后,试回答:
电解装置如图所示.图中B装置盛1L2mol?L-1的Na2SO4溶液,A装置中盛1L2mol?L-1 AgNO3溶液.通电后,湿润的淀粉KI试纸的C端变蓝色.电解一段时间后,试回答: