题目内容
50mL 18.4mol/L硫酸与足量的铜片加热反应,被还原的硫酸的物质的量是( )
| A、0.92mol |
| B、大于0.46mol 小于0.92mol |
| C、0.46mol |
| D、小于0.46mol |
考点:浓硫酸的性质
专题:氧族元素
分析:铜与浓硫酸加热时发生反应,随着反应的进行,浓硫酸的浓度逐渐减小,当成为稀硫酸是此反应停止.
解答:
解:50mL18.4mol/L的硫酸中n(H2SO4)=18.4mol/L×0.05L=0.92mol,假设50mL 18.4mol/L的硫酸中的硫酸分子全部与铜反应时,由Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O可知,作氧化剂的硫酸为0.46mol,起酸作用的硫酸0.46mol,随着反应的进行,浓硫酸溶液的浓度逐渐减小,当成为稀硫酸是此反应停止,所以作氧化剂的硫酸的物质的量小于0.46mol,即被还原的硫酸的物质的量小于0.46mol,
故选D.
| ||
故选D.
点评:本题考查氧化还原反应,为高频考点,把握发生的氧化还原反应及量的关系为解答的关键,注意稀硫酸与Cu不反应,题目难度不大.

练习册系列答案
相关题目
跟mg CO2中所含的氧原子数相等的KMnO4的量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列有关铁的叙述中,正确的是( )
①铁能被磁铁吸引 ②人体的血红蛋白中含有铁元素 ③铁在氧气中剧烈燃烧但不能与水蒸气反应.
①铁能被磁铁吸引 ②人体的血红蛋白中含有铁元素 ③铁在氧气中剧烈燃烧但不能与水蒸气反应.
| A、①② | B、①③ | C、②② | D、② |
下列的说法中正确的是( )
| A、钠的还原性很强,在空气中易变质,久置后变为过氧化钠 |
| B、氢氧化钠溶液可长时间保存在带磨口玻璃塞的试剂瓶中 |
| C、新制的氯水通常保存在棕色玻璃试剂瓶中,并现用现配 |
| D、漂粉精的有效成分为氯化钙 |
下列实验操作中错误的是( )
| A、蒸发操作时,当出现大量晶体是,才能停止加热,用余热加热 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、萃取操作时,应选择有机萃取剂,萃取剂的密度应比水大 |
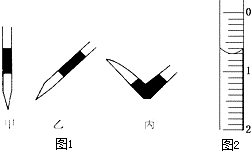 使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.
使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.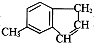 )是一种医药合成中间体,某同学设计它的合成路线如下:
)是一种医药合成中间体,某同学设计它的合成路线如下: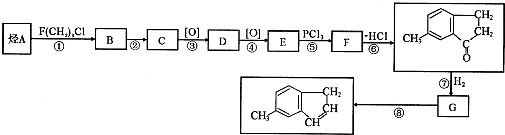
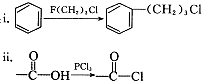
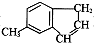 )的说法正确的是
)的说法正确的是