题目内容
跟mg CO2中所含的氧原子数相等的KMnO4的量为( )
A、
| ||
B、
| ||
C、
| ||
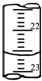
D、
|
考点:物质的量的相关计算
专题:计算题
分析:先根据n=
计算出二氧化碳的物质的量,再根据二氧化碳的化学式组成计算出氧原子的物质的量,然后根据高锰酸钾的化学式组成计算出需要高锰酸钾的物质的量.
| m |
| M |
解答:
解:mg二氧化碳的物质的量为:n(CO2)=
=
mol,含有氧原子的物质的量为:n(O)=2n(CO2)=
mol×2=
mol,
需要高锰酸钾的物质的量为:n(KMnO4)=
n(O)═
mol×
=
mol,
故选D.
| mg |
| 44g/mol |
| m |
| 44 |
| m |
| 44 |
| m |
| 22 |
需要高锰酸钾的物质的量为:n(KMnO4)=
| 1 |
| 4 |
| m |
| 22 |
| 1 |
| 4 |
| m |
| 88 |
故选D.
点评:本题考查了物质的量计算,题目难度中等,注意掌握物质的量与摩尔质量等物理量之间的关系,明确物质化学式与组成元素之间的关系为解答关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
下列说法正确的是( )
| A、需要加热的化学反应都是吸热反应 |
| B、原电池是将电能转化为化学能的一种装置 |
| C、物质的燃烧都是放热反应 |
| D、化学键的形成需吸收能量 |
下列有关硫的叙述中,不正确的是( )
| A、粘附在试管壁上的硫可用二硫化碳清洗 |
| B、S2和S8是同素异形体 |
| C、硫在自然界中主要以化合态形式存在 |
| D、硫粉和铜粉混合共热生成黑色的CuS |
利用“化学蒸汽转移法“可制备TaS2晶体,其逆反应为TaS2(s)+2I2(g)?TaI4(g)+S2(g),△H>0,在其他条件不变的情况下,下列关于该逆反应的说法正确的是( )
| A、加入催化剂,S2的物质的量增大 |
| B、改变压强,平衡不移动,反应吸收的热量不变 |
| C、升高温度,反应速率加快,反应吸收的热量不变 |
| D、向容器中加入TaS2可以提高I2的转化率 |
以Mg、MgO、Mg(OH)2、MgCO3、MgSO4、BaCl2溶液和盐酸为原料,直接制取M可有多种方法,其中运用复分解反应的( )
| A、二种 | B、三种 | C、四种 | D、五种 |
50mL 18.4mol/L硫酸与足量的铜片加热反应,被还原的硫酸的物质的量是( )
| A、0.92mol |
| B、大于0.46mol 小于0.92mol |
| C、0.46mol |
| D、小于0.46mol |
 某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下: