题目内容
13.下列各组中的反应,不属于同一反应类型的是( )| A. | 乙醇在一定条件下转化为乙醛,交警用K2Cr2O7检查司机是否酒驾 | |
| B. | 由甲苯硝化制对硝基甲苯,由苯甲酸乙酯水解制苯甲酸和乙醇 | |
| C. | 乙醇分子间脱水成乙醚,溴乙烷在一定条件下脱去HCl成乙烯 | |
| D. | 油酸甘油酯通过氢化反应转变为硬脂酸甘油酯,由丙烯与水反应制丙醇 |
分析 A.乙醇含有羟基,可发生取代、氧化反应;
B.硝化反应和水解反应都为取代反应;
C.乙醇发生取代反应生成乙醚,溴乙烷发生消去反应生成乙烯;
D.油脂的氢化为加成反应,丙烯与水发生加成反应生成丙醇.
解答 解:A.乙醇含有羟基,生成乙醛为氧化反应,与K2Cr2O7发生氧化反应,类型相同,故A不选;
B.甲苯的硝化反应以及苯甲酸乙酯的水解反应都为取代反应,故B不选;
C.乙醇发生取代反应生成乙醚,溴乙烷发生消去反应生成乙烯,反应类型不同,故C选;
D.油脂的氢化为加成反应,丙烯与水发生加成反应生成丙醇,反应类型相同,故D不选.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物中的官能团及官能团与性质的关系为解答的关键,侧重性质及有机反应类型的考查,题目难度不大.

练习册系列答案
相关题目
3.将一定量的SO2和O2放入一定体积的密闭容器中,500℃时,在催化剂作用下发生反应:2SO2(g)+O2(g)?2SO3(g),不能作为判断该反应达到平衡状态的标志是( )
| A. | 容器中气体密度保持不变 | |
| B. | 容器中混合气体的平均相对分子质量保持不变 | |
| C. | 容器中气体的压强保持不变 | |
| D. | 单位时间内,消耗amol O2的同时生成2amol SO2 |
4.以下是对某水溶液进行离子检验的方法和结论,其中正确的( )
| A. | 先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀.溶液中一定含有SO42- | |
| B. | 加入足量的HCl溶液,有气体产生,将气体通入澄清石灰水有白色沉淀.溶液中一定含有CO32- | |
| C. | 加入足量浓 NaOH溶液,产生了带有强烈刺激性气味的气体且该气体可以使湿润的红色石蕊试纸变蓝.溶液中一定含有NH4+ | |
| D. | 先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生白色沉淀.溶液中一定含有Cl- |
1.下列原子或离子原子核外电子排布不属于基态排布的是( )
| A. | Na 1s22s22p53s2 | B. | S2- 1s22s22p63s23p6 | ||
| C. | N 1s22s22p3 | D. | Si 1s22s22p63s23p2 |
18.等质量的下列各烃,完全燃烧后消耗氧气最多的是( )
| A. | C2H6 | B. | C2H4 | C. | C2H2 | D. | CH4 |
5.蛇纹石矿可看作由MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制碱式碳酸镁的实验步骤如下: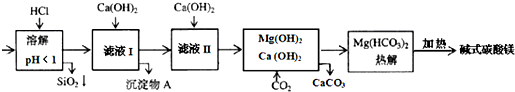
室温下,相关金属氢氧化物沉淀的KSP见下表
注:①lg2=0.3,②溶液中某离子的浓度小于1.0×10-5 mol•L-1,可认为该离子沉淀完全.
下列说法正确的是( )

室温下,相关金属氢氧化物沉淀的KSP见下表
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| (溶度积)KSP | 4.0×10-38 | 1.25×10-33 | 1.8×10-11 |
下列说法正确的是( )
| A. | 在滤液I中,加过量的Ca(OH)2使Fe3+和Al3+沉淀完全 | |
| B. | 滤液I中,加Ca(OH)2后Al3+比Fe3+先沉淀完全 | |
| C. | 室温下,用Ca(OH)2把滤液I的pH调节到4.7时,Al3+刚好沉淀完全 | |
| D. | 若碱式碳酸镁【aMgCO3•b Mg(OH)2】高温加热分解得到6.6g CO2和8.0g MgO,由此可知其化学式为MgCO3•3Mg(OH)2 |
2.下列叙述中正确的是( )
| A. | 可用丁达尔效应区别溶液和胶体 | B. | 稀硫酸不具有氧化性 | ||
| C. | 光导纤维的主要成分是硅 | D. | 石油的分馏属于化学变化 |
