题目内容
4.以下是对某水溶液进行离子检验的方法和结论,其中正确的( )| A. | 先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀.溶液中一定含有SO42- | |
| B. | 加入足量的HCl溶液,有气体产生,将气体通入澄清石灰水有白色沉淀.溶液中一定含有CO32- | |
| C. | 加入足量浓 NaOH溶液,产生了带有强烈刺激性气味的气体且该气体可以使湿润的红色石蕊试纸变蓝.溶液中一定含有NH4+ | |
| D. | 先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生白色沉淀.溶液中一定含有Cl- |
分析 A.该白色沉淀可能为氯化银,原溶液中可能存在银离子,不一定含有硫酸根离子;
B.可能含有HCO3-;
C.使湿润的红色石蕊试纸变蓝的气体为氨气;
D.加入盐酸,引入氯离子.
解答 解:A.向某溶液中加入氯化钡溶液,有白色沉淀生成,再加硝酸酸化,沉淀不溶解,该白色沉淀可能为氯化银,原溶液中可能含有银离子,不一定含有硫酸根离子,故A错误;
B.加入盐酸生成能时澄清石灰水变浑浊的气体,如为二氧化碳气体,也可能含有HCO3-,故B错误;
C.使湿润的红色石蕊试纸变蓝的气体为氨气,可用铵根离子与氢氧化钠反应生成生成,可用于检验铵根离子,故C正确;
D.此溶液利用盐酸酸化,此时引入离子氯离子,不能证明原溶液中存在氯离子,故D错误;
故选C.
点评 本题考查离子的检验,为高考常见题型和高频考点,题目难度不大,注意多积累常见离子的检验方法,做题时注意排除其它离子的干扰,试题贴近高考,针对性强;有利于激发学生的学习兴趣和学习积极性.

练习册系列答案
相关题目
15.${\;}_{6}^{13}$C-NMR(核磁共振)可用于含碳化合物的结构分析,${\;}_{6}^{13}$C表示的含义错误的是( )
| A. | ${\;}_{6}^{13}$C原子内的中子数为6 | B. | ${\;}_{6}^{13}$C核外电子数为6 | ||
| C. | ${\;}_{6}^{13}$C质量数为13 | D. | ${\;}_{6}^{13}$C与$\frac{12}{6}$C互为同位素 |
13.下列各组中的反应,不属于同一反应类型的是( )
| A. | 乙醇在一定条件下转化为乙醛,交警用K2Cr2O7检查司机是否酒驾 | |
| B. | 由甲苯硝化制对硝基甲苯,由苯甲酸乙酯水解制苯甲酸和乙醇 | |
| C. | 乙醇分子间脱水成乙醚,溴乙烷在一定条件下脱去HCl成乙烯 | |
| D. | 油酸甘油酯通过氢化反应转变为硬脂酸甘油酯,由丙烯与水反应制丙醇 |
14.对于某一化学反应,下列各项反应条件改变,能增大单位体积内活化分子百分数,降低化学反应的活化能,从而提高反应速率的是( )
| A. | 增大反应物浓度 | B. | 加压 | C. | 升温 | D. | 加催化剂 |
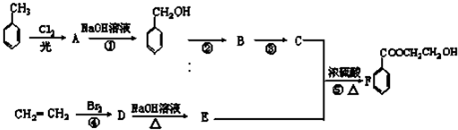
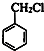 DBrCH2CH2Br
DBrCH2CH2Br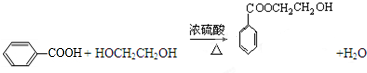 .
. ,该主要成分完全燃烧的化学方程式CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
,该主要成分完全燃烧的化学方程式CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.