题目内容
20.氢氧燃料电池,电极为多孔镍,电解质溶液为30%的KOH溶液,电池总反应为2H2+O2═2H2O,该电池工作时,下列说法正确的是( )①负极质量减轻
②负极反应为O2+2H2O+4e-═4OH-
③负极反应为2H2+4OH--4e-═4H2O
④正极区pH升高,而负极区pH降低
⑤溶液中阴离子移向负极.
| A. | ①③④ | B. | ②③⑤ | C. | ③④⑤ | D. | ④⑤ |
分析 氢氧燃料电池工作时,通入氢气的一极为电池的负极,负极上氢气失电子生成水,通入氧气的一极为电池的正极,正极上氧气得电子生成氢氧根离子,溶液中阴离子向负极移动,据此分析.
解答 解:①通入氢气的一极为电池的负极,负极上氢气失电子生成水,负极电极材料不参加反应,故错误;
②通入氢气的一极为电池的负极,负极上氢气失电子生成水,负极反应为2H2+4OH--4e-═4H2O,故错误;
③通入氢气的一极为电池的负极,负极上氢气失电子生成水,负极反应为2H2+4OH--4e-═4H2O,故正确;
④通入氧气的一极为电池的正极,正极上氧气得电子生成氢氧根离子,正极反应式O2+2H2O+4e-═4OH-,所以正极区pH升高,而负极反应为2H2+4OH--4e-═4H2O,则负极区pH降低,故正确;
⑤氢氧燃料电池工作时,溶液中阴离子移向负极,故正确.
故选C.
点评 本题考查原电池的组成以及工作原理,题目难度不大,注意电极反应式的书写以及电解质溶液对电极方程式的影响.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
10.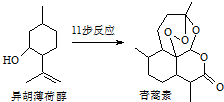 2015年诺贝尔生理学、医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素.以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如图).下列说法正确的是( )
2015年诺贝尔生理学、医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素.以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如图).下列说法正确的是( )
 2015年诺贝尔生理学、医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素.以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如图).下列说法正确的是( )
2015年诺贝尔生理学、医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素.以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如图).下列说法正确的是( )| A. | 异胡薄荷醇的分子式为C10H12O | |
| B. | 青蒿素提取时可以通过加热或加碱溶解的方法提高其浸取率 | |
| C. | 青蒿素易溶于水,而难溶于有机溶剂 | |
| D. | 异胡薄荷醇可发生消去反应 |
15.下列各表述与示意图一致的是( )


| A. | 图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积的关系图.则三种离子的物质的量之比为:n(Mg2+):n(Al3+):n( NH4+)=2:3:2 | |
| B. | 图①中使用的NaOH的浓度为2 mol/L | |
| C. | 图②表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| D. | 图③中曲线表示3H2(g)+N2(g)═2NH3(g)反应过程的能量变化.若使用催化剂,B点会降低 |
5.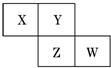 X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
 X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )| A. | X的最常见气态氢化物的水溶液显酸性 | |
| B. | 最高价氧化物对应水化物的酸性W比Z强 | |
| C. | Z的单质与氢气反应比Y单质与氢气反应剧烈 | |
| D. | X的原子半径小于Y |
12.我国古代发明或技术应用中,其工作原理不涉及化学反应的是
①指南针②黑火药③转轮排字④黏土制陶瓷⑤用玻璃瓶盛装“强水”(古书中记载一种能腐蚀五金的液体⑥用明矾溶液清洗铜镜表面的铜锈⑦湿法炼铜( )
①指南针②黑火药③转轮排字④黏土制陶瓷⑤用玻璃瓶盛装“强水”(古书中记载一种能腐蚀五金的液体⑥用明矾溶液清洗铜镜表面的铜锈⑦湿法炼铜( )
| A. | ①③④⑤ | B. | ①③⑤ | C. | ①③④⑦ | D. | ①③⑤⑥ |
10.我国硫酸工业制取二氧化硫的主要反应为4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$8SO2+2Fe2O3,其中FeS2是( )
| A. | 还原剂 | B. | 氧化剂 | ||
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂又不是还原剂 |
 .
. 、
、 .
.