题目内容
①CaCO3(s)═CaO+CO2(g);△H=177.7kJ/mol
②C(s)+H2O(g)═CO(g)+H2(g);△H=-131.3kJ/mol
③0.5H2SO4(l)+NaOH(l)═0.5Na2SO4(l)+H2O(l);△H=-57.3kJ/mol
④C(s)+O2(g)═CO2(g);△H=-393.5kJ/mol
⑤CO(g)+1/2O2(s)═CO2(g);△H=-283kJ/mol
⑥HNO3 (aq)+NaOH(aq)═NaNO3(aq)+H2O(l);△H=-57.3kJ/mol
⑦2H2(g)+O2(g)═2H2O(l);△H=-517.6kJ/mol
(1)上述热化学方程式中,不正确的有 ,不正确的理由分别是 ;
(2)根据上述信息,写出C转化为CO的热化学方程式 .
②C(s)+H2O(g)═CO(g)+H2(g);△H=-131.3kJ/mol
③0.5H2SO4(l)+NaOH(l)═0.5Na2SO4(l)+H2O(l);△H=-57.3kJ/mol
④C(s)+O2(g)═CO2(g);△H=-393.5kJ/mol
⑤CO(g)+1/2O2(s)═CO2(g);△H=-283kJ/mol
⑥HNO3 (aq)+NaOH(aq)═NaNO3(aq)+H2O(l);△H=-57.3kJ/mol
⑦2H2(g)+O2(g)═2H2O(l);△H=-517.6kJ/mol
(1)上述热化学方程式中,不正确的有
(2)根据上述信息,写出C转化为CO的热化学方程式
考点:反应热和焓变,热化学方程式
专题:化学反应中的能量变化
分析:(1)热化学方程式要标明物质的聚集状态,并且焓变的符号和单位要正确,根据热化学方程式的书写方法来回答;
(2)结合化学反应④⑤,利用盖斯定律来回答.
(2)结合化学反应④⑤,利用盖斯定律来回答.
解答:
解:(1)根据热化学方程式的书写方法,①②③都是有错误的,错误之处分别是:①中CaO没标状态,△H=+177.7/mol,②的状态应为“g”,△H=+131.KJ/mol,③除H2O外其它物质的状态不是“l”应为“aq”;
故答案为:①②③;①中CaO没标状态,②是吸热反应,△H=+131.KJ/mol;③除H2O外其它物质的状态不是“l”应为“aq”;
(2)结合化学反应④⑤,利用盖斯定律,反应C(s)+
O2(g)=CO(g)是④-⑤得来,所以焓变△H=-110.5KJ/mol,故答案为:C(s)+
O2(g)=CO(g)△H=-110.5KJ/mol.
故答案为:①②③;①中CaO没标状态,②是吸热反应,△H=+131.KJ/mol;③除H2O外其它物质的状态不是“l”应为“aq”;
(2)结合化学反应④⑤,利用盖斯定律,反应C(s)+
| 1 |
| 2 |
| 1 |
| 2 |
点评:本题考查学生热化学方程式的书写方法以及盖斯定律计算等知识,注意知识的归纳和整理是解题关键,难度不大.

练习册系列答案
相关题目
下列说法中不正确的是( )
| A、淀粉和纤维素的化学式都是(C6H10O5)n,但由于n不同,淀粉和纤维素并不互为同分异构体 |
| B、鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可用灼烧的方法 |
| C、乙醇可以被酸性高锰酸钾溶液或酸性重铬酸钾溶液直接氧化成乙酸 |
| D、醇CH3CHOHCH3不能在铜或银作催化剂的条件下发生催化氧化反应 |
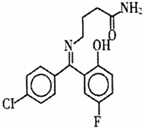 普罗加比对癫痫、痉挛和运动失调均有良好的治疗效果,其结构如图所示,有关普罗加比的说法正确的是( )
普罗加比对癫痫、痉挛和运动失调均有良好的治疗效果,其结构如图所示,有关普罗加比的说法正确的是( )| A、该分子在1H核磁共振谱中有12个峰 |
| B、一定条件下,1 mol普罗加比最多能与2 mol H2发生加成反应 |
| C、久置在空气中的普罗加比会因氧化而变质 |
| D、普罗加比可以和NaOH溶液、Na2CO3溶液反应,也可以和盐酸反应 |
以下物质不能通过化合反应实现的是( )
| A、NaHCO3 |
| B、Fe(OH)3 |
| C、Cu(OH)2 |
| D、FeCl2 |
下列物质的用途与其性质的对应关系错误的是( )
| A、氯气用于自来水消毒--次氯酸的强氧化性 |
| B、溴化银用于照相术--光照分解 |
| C、氢氟酸腐蚀玻璃--强酸性 |
| D、碘化银用于人工降雨--使空气中水蒸汽凝聚 |
下列说法中正确的是( )
| A、物质发生化学反应时都伴随着能量变化,伴随能量变化的物质变化一定是化学变化 |
| B、需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应 |
| C、吸热反应就是反应物的总能量比生成物的总能量高;也可以理解为化学键断裂时吸收的能量比化学键形成时放出的能量多 |
| D、因为3O2═2O3是吸热反应,所以臭氧比氧气的化学性质更活泼 |
下列物质中能导电的是( )
| A、熔融的氯化钠 | B、硝酸钾粉末 |
| C、硫酸铜晶 | D、无水乙醇 |
用NA表示阿伏加德罗常数,下列有关叙述正确的是( )
| A、2.24L CO2中含有的原子数为0.3NA |
| B、500mL 0.2mol/L的Fe2(SO4)3溶液中Fe3+总数为0.2NA |
| C、5.6g铁粉与硝酸完全反应失去的电子数一定为0.3NA |
| D、28g N2和CO的混合气体含有的原子总数为2NA |