题目内容
现有含NaCl、MgCl2和CaCl2的混合溶液,某兴趣小组的同学欲提取纯净的NaCl晶体,设计了如下实验:
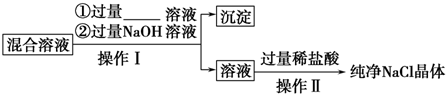
请回答下列问题:
(1)写出沉淀中所含物质的化学式: ,①中加入的过量试剂为 .
(2)上述流程中,加入过量稀盐酸的目的是 .
(3)操作Ⅰ、Ⅱ中均需使用的玻璃仪器是 ,该仪器在操作Ⅰ、Ⅱ中的作用分别是:Ⅰ ,Ⅱ .

请回答下列问题:
(1)写出沉淀中所含物质的化学式:
(2)上述流程中,加入过量稀盐酸的目的是
(3)操作Ⅰ、Ⅱ中均需使用的玻璃仪器是
考点:粗盐提纯
专题:实验题
分析:含NaCl、MgCl2和CaCl2的混合溶液,加入过量的碳酸钠溶液,除去溶液中的钙离子,然后加入过量的氢氧化钠,除去溶液中的镁离子,过滤后得到的沉淀为碳酸钙和氢氧化镁的混合物,溶液中含有氯化钠、碳酸钠、氢氧化钠,要得到纯净的氯化钠晶体,应加入足量的稀盐酸除去碳酸根离子和氢氧根离子,盐酸中的氯化氢易挥发,加热可以除去,在过滤中需要用过滤棒引流待虑液体,在蒸发结晶过程中用玻璃棒搅拌溶液,使其受热均匀.
解答:
解:(1)含NaCl、MgCl2和CaCl2的混合溶液,加入过量的碳酸钠溶液,除去溶液中的钙离子,然后加入过量的氢氧化钠,除去溶液中的镁离子,过滤后得到的沉淀为碳酸钙和氢氧化镁的混合物,
故答案:Mg(OH)2 CaCO3;Na2CO3;
(2)溶液中含有氯化钠、碳酸钠、氢氧化钠,要得到纯净的氯化钠晶体,应加入足量的稀盐酸除去碳酸根离子和氢氧根离子,盐酸中的氯化氢易挥发,加热可以除去,所以加入过量稀盐酸的目的是除去溶液中过量的OH-和CO32-,
故答案为:除去溶液中过量的OH-和CO32-;
(3)在过滤中需要用过滤棒引流待虑液体,在蒸发结晶过程中用玻璃棒搅拌溶液,使其受热均匀,
故答案为:玻璃棒;引流;搅拌.
故答案:Mg(OH)2 CaCO3;Na2CO3;
(2)溶液中含有氯化钠、碳酸钠、氢氧化钠,要得到纯净的氯化钠晶体,应加入足量的稀盐酸除去碳酸根离子和氢氧根离子,盐酸中的氯化氢易挥发,加热可以除去,所以加入过量稀盐酸的目的是除去溶液中过量的OH-和CO32-,
故答案为:除去溶液中过量的OH-和CO32-;
(3)在过滤中需要用过滤棒引流待虑液体,在蒸发结晶过程中用玻璃棒搅拌溶液,使其受热均匀,
故答案为:玻璃棒;引流;搅拌.
点评:本题考查了粗盐提纯操作步骤及玻璃棒的作用,试题难度不大,试题侧重对学生基础知识的巩固和训练,提高学生分析问题、解决问题的能力.

练习册系列答案
相关题目
关于下列四个装置的说明符合实验要求的是( )
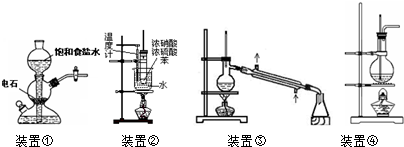

| A、装置①:实验室中若需制备较多量的乙炔可用此装置 |
| B、装置②:实验室中可用此装置来制备硝基苯,但产物中可能会混有苯磺酸 |
| C、装置③:实验室中可用此装置来分离含碘的四氯化碳液体,最终在锥型瓶中可获得碘 |
| D、装置④:实验室中可用此装置来制备乙酸乙酯并在烧瓶中获得产物 |
