题目内容
水是人体最不可缺的物质,已知水的电离方程式:H2O?H++OH-
金属钠可以和冷水剧烈反应
(1)写出一绿豆粒大小金属钠投入水中反应的化学方程式,并标出电子转移的方向和数目. ,氧化剂是 ;还原产物的摩尔质量为 .
(2)在反应整个过程中:
①受到破坏的化学键有 ;
②水的电离平衡受到: .
A.促进 B.抑制 C.先促进后抑制 D.先抑制后促进
(3)比较金属钠与水、无水乙醇、乙酸溶液反应速率的快慢顺序 .
金属钠可以和冷水剧烈反应
(1)写出一绿豆粒大小金属钠投入水中反应的化学方程式,并标出电子转移的方向和数目.
(2)在反应整个过程中:
①受到破坏的化学键有
②水的电离平衡受到:
A.促进 B.抑制 C.先促进后抑制 D.先抑制后促进
(3)比较金属钠与水、无水乙醇、乙酸溶液反应速率的快慢顺序
考点:氧化还原反应的电子转移数目计算,化学键,氧化还原反应,水的电离
专题:基本概念与基本理论
分析:(1)金属钠和水之间反应生成氢氧化钠和氢气,化合价升高元素失电子,此元素在产物是氧化产物,化合价降低元素得电子,所在反应物是氧化剂,得电子数=失电子数=转移电子数;
(2)金属钠参与反应,金属键遭到破坏,水分子中的化学键也受到破坏,消耗水,实质是和水中的氢离子之间反应;
(3)物质电离出氢离子的能力越强,则和金属钠的反应越剧烈.
(2)金属钠参与反应,金属键遭到破坏,水分子中的化学键也受到破坏,消耗水,实质是和水中的氢离子之间反应;
(3)物质电离出氢离子的能力越强,则和金属钠的反应越剧烈.
解答:
解:(1)金属钠和水之间反应生成氢氧化钠和氢气,化合价升高元素Na的原子失电子,此元素在产物NaOH是氧化产物,化合价降低H元素的原子得电子,所在反应物氢气是氧化剂,得电子数=失电子数=转移电子数,电子转移如下: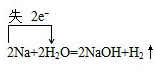 ,反应中H2O是氧化剂,氢气是还原产物,摩尔质量是:2g/mol,故答案为:
,反应中H2O是氧化剂,氢气是还原产物,摩尔质量是:2g/mol,故答案为: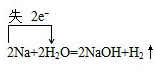 ;H2O;2g/mol;
;H2O;2g/mol;
(2)①金属钠参与反应,其中的金属键遭到破坏,水分子中的极性共价键也受到破坏,故答案为:(极性)共价键、金属键;
②金属钠和水反应,实质是和水中的氢离子之间反应,促使水的电离平衡正向移动,故答案为:A;
(3)电离出氢离子的能力:乙酸>水>乙醇,金属钠与水、无水乙醇、乙酸溶液反应速率的快慢顺序是:乙酸>水>乙醇.
故答案为:乙酸>水>乙醇.
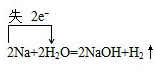 ,反应中H2O是氧化剂,氢气是还原产物,摩尔质量是:2g/mol,故答案为:
,反应中H2O是氧化剂,氢气是还原产物,摩尔质量是:2g/mol,故答案为: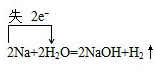 ;H2O;2g/mol;
;H2O;2g/mol;(2)①金属钠参与反应,其中的金属键遭到破坏,水分子中的极性共价键也受到破坏,故答案为:(极性)共价键、金属键;
②金属钠和水反应,实质是和水中的氢离子之间反应,促使水的电离平衡正向移动,故答案为:A;
(3)电离出氢离子的能力:乙酸>水>乙醇,金属钠与水、无水乙醇、乙酸溶液反应速率的快慢顺序是:乙酸>水>乙醇.
故答案为:乙酸>水>乙醇.
点评:本题以金属钠和水的反应为载体,涉及氧化还原反应、化学键、电子转移等知识的考查,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
相关题目
常温下,0.1mol/L的HA溶液中
=1×10-8,下列叙述中正确的是( )
| c(OH-) |
| c(H+) |
| A、该溶液中由水电离产生的c(H+)=1×10-8mol/L |
| B、0.01mol/LHA的溶液中c(H+)=1×10-4mol/L |
| C、1体积pH=3的HA与10体积pH=11的NaOH混合后溶液中c(OH-)+c(A-)═c(H+)+c(Na+) |
| D、浓度均为0.1 mol/L的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(OH-)-c(H+)<c(HA)-c(A-) |
下列说法正确的是( )
| A、用纸上层析法分离和检验墨水的成分,为了看到色斑,只有有色离子的检验才可以用纸层析法 |
| B、容量瓶、量筒、滴定管上都具体标明使用温度,容量瓶有标线无“0”刻度,量筒、滴定管都有“0”刻度;使用时容量瓶水洗后不用润洗,量筒、滴定管水洗后还需润洗 |
| C、溴水中加入苯,溴水褪色了是因为溴与苯发生了取代反应,溴水中通入乙烯,溴水褪色了是因为溴与乙烯发生了加成反应 |
| D、物质的分离提纯方法之一为“筛分”:如胶体-渗析法分离提纯;浊液-过滤分离,本质上就是依据所分离粒子的直径大小选择具有合适孔径的“筛子” |
化学在工业生产和日常生活中都有着重要的应用,下列说法正确的是( )
| A、活性炭、SO2、氯水都会因发生氧化还原反应而使品红溶液褪色 |
| B、Na2O2、H2O2所含化学键完全相同,都能作供氧剂 |
| C、常温下,浓硫酸、浓硝酸与铝均能发生钝化,均能用铝罐储运 |
| D、水玻璃,从分类法的角度,可看作纯净物,可用于木材等的防火剂 |
下列图示与对应的叙述不相符的是( )
A、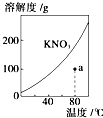 如图表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
B、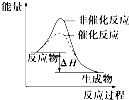 如图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
C、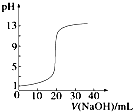 如图表示0.1000mol?L-1 NaOH溶液滴定20.00mL 0.1000mol?L-1醋酸溶液得到的滴定曲线 |
D、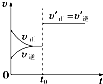 如图表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件可能是增大压强 |
 Ⅰ.CN-能与Ni2+形成[Ni(CN)4]2-配离子
Ⅰ.CN-能与Ni2+形成[Ni(CN)4]2-配离子