题目内容
16.下列说法中正确的是( )| A. | 电解质在固态时均为离子晶体 | |
| B. | CCl4、Cl2及HF中的原子都满足最外层8电子稳定结构 | |
| C. | 用道尔顿的原子结构理论无法解释同位素现象 | |
| D. | 晶体类型相同,则晶体中化学键也完全相同 |
分析 A.纯净的电解质在固态时可能属于分子晶体;
B.在ABn型分子中,如果A原子的最外层电子数+成键电子数=8,则该化合物中所有原子都达到8电子结构,但氢化物除外;
C.1808年,英国科学家道尔顿提出了原子论.他认为物质都是由原子直接构成的;原子是一个实心球体,不可再分割;同一类原子性质相同;不同的原子是以简单的整数比相结合;
D.氯化钠和过氧化钠都是离子晶体,但氯化钠中只有离子键,而过氧化钠中存在共价键和离子键.
解答 解:A.纯净的电解质在固态时可能属于分子晶体,如冰醋酸,故A错误;
B.在ABn型分子中,如果A原子的最外层电子数+成键电子数=8,则该化合物中所有原子都达到8电子结构,但HF中的氢是两电子的稳定结构,故B错误;
C.1808年,英国科学家道尔顿提出了原子论.他认为物质都是由原子直接构成的;原子是一个实心球体,不可再分割;同一类原子性质相同;不同的原子是以简单的整数比相结合,所以用道尔顿的原子结构理论无法解释同位素现象,故C正确;
D.氯化钠和过氧化钠都是离子晶体,但氯化钠中只有离子键,而过氧化钠中存在共价键和离子键,所以晶体类型相同,则晶体中化学键并不一定完全相同,故D错误;
故选C.
点评 本题考查了化学键、8电子结构等知识点,根据物质的构成微粒判断化学键,知道8电子结构的判断方法,题目难度不大.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
7.下列化学用语正确的是( )
| A. | Zn的电子排布式:1s22s22p63s23p64s2 | |
| B. | Fe2+的原子结构示意图: | |
| C. | C的价电子轨道表示式: | |
| D. | HClO的电子式: |
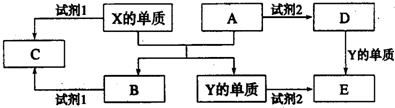
8.已知甲、乙、丙三种物质均含有同种元素X,其转化关系如下:

下列说法错误的是( )

下列说法错误的是( )
| A. | 若A为NaOH溶液,乙为白色沉淀,则X可能为短周期金属元素 | |
| B. | 若A为硝酸,X为金属元素,则甲与乙反应可生成丙 | |
| C. | 若A为氧气,丙在通常状况下为红棕色气体,则甲可能为非金属单质 | |
| D. | 若乙为NaHCO3,则甲或丙可能是CO2 |
4.将少量CO2气体通入下列物质的水溶液中,不会产生沉淀的是( )
| A. | CaCl2 | B. | Ca(OH)2 | C. | 饱和Na2CO3溶液 | D. | Ca(ClO)2 |
11.下列离子反应方程式正确的是( )
| A. | 向Ca(ClO)2溶液中通入少量SO2:Ca2++3ClO-+SO2+H2O═CaSO3↓+Cl-+2HClO | |
| B. | 1 mol/L的NaAlO2溶液和2.5 mol/L的盐酸等体积均匀混合:2AlO2-+5H+═Al(OH)3↓+Al3++H2O | |
| C. | 将11.2L标准状况下的氯气通入200mL2mol/L的FeBr2溶液中,离子反应方程式为:2Fe2++8Br-+5Cl2═2Fe3++4Br2+10Cl- | |
| D. | 氢氧化亚铁溶于稀硝酸中:Fe(OH)2+2H+═Fe2++2H2O |
1.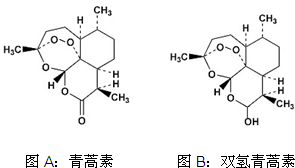 中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖.下列有关青蒿素和双氢青蒿素(结构分别为图A、图B)的说法中不正确的是( )
中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖.下列有关青蒿素和双氢青蒿素(结构分别为图A、图B)的说法中不正确的是( )
 中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖.下列有关青蒿素和双氢青蒿素(结构分别为图A、图B)的说法中不正确的是( )
中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖.下列有关青蒿素和双氢青蒿素(结构分别为图A、图B)的说法中不正确的是( )| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 由青蒿素制备双氢青蒿素的反应属还原反应 | |
| C. | 青蒿素分子中含有过氧键和酯基、醚键 | |
| D. | 双氢青蒿素分子中有2个六元环和2个七元环 |
5.如图是某学校实验室从化学试剂商店买的98%硫酸试剂标签上的部分内容.据此下列说法正确的是( )


| A. | 该硫酸的物质的量浓度为1.84mol/L | |
| B. | 若 Zn与该硫酸反应消耗13克Zn,一定产生4.48升气体 | |
| C. | 配制200mL 4.6mol/L的稀硫酸需取该硫酸50mL | |
| D. | 该硫酸与等体积的水混合所得溶液的物质的量浓度等于9.2mol/L |
6.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 2L 1mol/L Na2SO4溶液中离子总数为3NA | |
| B. | 25℃、101.3kPa时,11.2L H2中含有的原子数为NA | |
| C. | 4℃、101.3kPa时,54mL H2O中含有的原子数为3NA | |
| D. | 78g Na2O2与足量水充分反应时电子转移数为NA |