题目内容
4.将少量CO2气体通入下列物质的水溶液中,不会产生沉淀的是( )| A. | CaCl2 | B. | Ca(OH)2 | C. | 饱和Na2CO3溶液 | D. | Ca(ClO)2 |
分析 A.二氧化碳和氯化钙溶液不发生反应;
B.二氧化碳与氢氧化钙反应生成碳酸钙;
C.二氧化碳与饱和碳酸钠溶液反应,析出碳酸氢钠;
D.发生反应:CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO.
解答 解:A.盐酸是强酸,碳酸是弱酸,所以碳酸不能制取盐酸,即二氧化碳和氯化钙不反应,最终没有沉淀析出,故A正确;
B.二氧化碳与氢氧化钙反应生成碳酸钙,碳酸钙属于难溶电解质,所以把少量CO2气体通入Ca(OH)会生成碳酸钙白色沉淀,故B错误;
C.二氧化碳与饱和碳酸钠溶液反应,析出碳酸氢钠,碳酸氢钠的溶解度比碳酸钠的小,故C错误;
D.发生反应:CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO,生成碳酸钙沉淀,故D错误.
故选A.
点评 本题考查了离子反应发生的条件,题目难度不大,试题注重了基础知识的考查,注意明确离子反应发生的条件、掌握常见元素化合物的化学性质.

练习册系列答案
相关题目
15.两种金属粉末的混合物9g与足量的稀硫酸反应收集到标准状况下的氢气6.72L,则这种混合物的可能组成是( )
| A. | Mg和Al | B. | Fe和Zn | C. | Fe和Cu | D. | Fe和Al |
16.下列离子方程式正确的是( )
| A. | 向碘化亚铁溶液中滴加溴的四氯化碳溶液2Br2+2Fe2++2I-═I2+4Br-+2Fe3+ | |
| B. | 向含等物质的量浓度AgNO3和Cu(NO3)2的溶液中缓慢加入镁粉4Cu2++2Ag++5Mg═4Cu+2Ag+5Mg2+ | |
| C. | 氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O | |
| D. | 向0.3mol/LNaClO溶液中滴加等体积的0.2mol/LNaHSO3溶液:2HSO3-+4ClO-═2SO42-+2Cl-+2HClO |
9.下列有关实验的说法不正确的是( )
| A. | 铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面形成了一层致密稳定的氧化膜 | |
| B. | 实验室里吸入刺激性的氯气、氯化氢气体中毒时,吸入少量酒精或乙醚的混合蒸气解毒 | |
| C. | SO2的水溶液和苯溶液中分别通入溴水褪色,两者的原理一样 | |
| D. | 在蛋白质溶液中加入氯化钡有沉淀产生,是因为蛋白质变性 |
16.下列说法中正确的是( )
| A. | 电解质在固态时均为离子晶体 | |
| B. | CCl4、Cl2及HF中的原子都满足最外层8电子稳定结构 | |
| C. | 用道尔顿的原子结构理论无法解释同位素现象 | |
| D. | 晶体类型相同,则晶体中化学键也完全相同 |
13.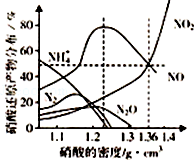 某些金属与不同密度的硝酸反应时,往往生成多种不同价态的还原产物,如图是在相同条件下,各种不同密度的硝酸和铁反应时,还原产物的分布图.通过图象判断下列说法错误的是( )
某些金属与不同密度的硝酸反应时,往往生成多种不同价态的还原产物,如图是在相同条件下,各种不同密度的硝酸和铁反应时,还原产物的分布图.通过图象判断下列说法错误的是( )
 某些金属与不同密度的硝酸反应时,往往生成多种不同价态的还原产物,如图是在相同条件下,各种不同密度的硝酸和铁反应时,还原产物的分布图.通过图象判断下列说法错误的是( )
某些金属与不同密度的硝酸反应时,往往生成多种不同价态的还原产物,如图是在相同条件下,各种不同密度的硝酸和铁反应时,还原产物的分布图.通过图象判断下列说法错误的是( )| A. | 稀硝酸与铁反应,一定有NO生成 | |
| B. | 密度小于1.1g•cm-3的硝酸与铁反应,还原产物百分率最多的是NH4+ | |
| C. | 某硝酸试剂瓶的标签注明:密度为1.26g•cm-3,质量分数50.0%;若取该试剂10ml配成100ml溶液,所得溶液C(H+)=0.1 | |
| D. | 当硝酸的密度为1.36g•cm-3时,过量铁与硝酸反应,消耗的铁与被还原的硝酸物质的量之比为1:1 |
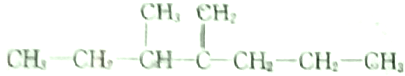 ,此烃名称为3-甲基-2-丙基-1-戊烯
,此烃名称为3-甲基-2-丙基-1-戊烯 ,可命名为1-甲基-3-乙基苯.
,可命名为1-甲基-3-乙基苯.