题目内容
我国第四套人民币硬币从1999年开始发行,一元币为钢芯镀镍(Ni),伍角币为钢芯镀铜合金,一角币为铝合金或不锈钢.
(1)铸造以上硬币用到的材料都是 (填“合成材料”或“金属材料”).
(2)选择铸造硬币的材料不需要考虑的因素是 (填序号).
A.金属的导电性 B.金属的耐腐蚀性C.金属的硬度 D.金属价格与硬币面值的吻合度
(3)以上硬币涉及到Fe、Cu、Al、Ni(镍),已知Ni能够发生如下反应:Ni+H2SO4=NiSO4+H2↑
Fe+NiCl 2=Ni+FeCl2
这两个反应的基本类型都是 .四种金属活动性由强到弱的顺序为 (用元素符号表示).
(1)铸造以上硬币用到的材料都是
(2)选择铸造硬币的材料不需要考虑的因素是
A.金属的导电性 B.金属的耐腐蚀性C.金属的硬度 D.金属价格与硬币面值的吻合度
(3)以上硬币涉及到Fe、Cu、Al、Ni(镍),已知Ni能够发生如下反应:Ni+H2SO4=NiSO4+H2↑
Fe+NiCl 2=Ni+FeCl2
这两个反应的基本类型都是
考点:金属与合金在性能上的主要差异,化学基本反应类型,常见金属的活动性顺序及其应用
专题:
分析:(1)依据硬币的组成成分分析材料的种类;
(2)根据硬币的流通特点分析硬币应具有的特点要求,特别是其耐腐蚀、硬度、及价值的相关因素;
(3)根据金属活动性顺序的具体应用对金属的活动性进行分析,依据反应的反应物生成物种类判断反应的类型.
(2)根据硬币的流通特点分析硬币应具有的特点要求,特别是其耐腐蚀、硬度、及价值的相关因素;
(3)根据金属活动性顺序的具体应用对金属的活动性进行分析,依据反应的反应物生成物种类判断反应的类型.
解答:
解:(1)根据题干所知硬币的组成成分都是金属的合金,所以铸造以上硬币用到的材料都是金属材料,故答案为:金属材料;
(2)根据硬币的流通特点可知:铸造出的硬币要有较强的耐腐蚀性、硬度较大、且硬币价值与面值的吻合度要接近,而金属的导电性不是铸造硬币所考虑的因素,故答案为:A;
(3)由金属活动性顺序的具体应用可知:活动性在氢前的金属可以与稀酸反应生成氢气,金属活动性强的金属可以把金属活动性比它弱的金属从其盐溶液中置换出来,所以根据Ni+H2SO4=NiSO4+H2↑
Fe+NiCl 2=Ni+FeCl2
可知:Ni活动性在氢前且比铁弱,结合金属活动性顺序表可知四种金属的活动性顺序是:Al>Fe>Ni>Cu,从反应类型上看Ni+H2SO4=NiSO4+H2↑
Fe+NiCl 2=Ni+FeCl2都是一种单质与一种化合物反应生成另一种单质与另一种化合物,故都是置换反应,故答案为:置换反应;Al>Fe>Ni>Cu.
(2)根据硬币的流通特点可知:铸造出的硬币要有较强的耐腐蚀性、硬度较大、且硬币价值与面值的吻合度要接近,而金属的导电性不是铸造硬币所考虑的因素,故答案为:A;
(3)由金属活动性顺序的具体应用可知:活动性在氢前的金属可以与稀酸反应生成氢气,金属活动性强的金属可以把金属活动性比它弱的金属从其盐溶液中置换出来,所以根据Ni+H2SO4=NiSO4+H2↑
Fe+NiCl 2=Ni+FeCl2
可知:Ni活动性在氢前且比铁弱,结合金属活动性顺序表可知四种金属的活动性顺序是:Al>Fe>Ni>Cu,从反应类型上看Ni+H2SO4=NiSO4+H2↑
Fe+NiCl 2=Ni+FeCl2都是一种单质与一种化合物反应生成另一种单质与另一种化合物,故都是置换反应,故答案为:置换反应;Al>Fe>Ni>Cu.
点评:本题考查合金以及金属活泼性,难度不大,解题的关键是充分理解和掌握金属活动性顺序表的意义以及其它相关的知识.

练习册系列答案
相关题目
下列有关实验现象的描述中,不正确的是( )
| A、灼烧Na与NaCl时,火焰颜色均显黄色 |
| B、钠在空气中燃烧后得到白色固体 |
| C、钠投入硫酸铜溶液中,会产生蓝色沉淀 |
| D、饱和碳酸钠溶液中滴加酚酞试液,溶液变红色 |
下列关于氯水的叙述中,正确的是( )
| A、新制氯水中只含Cl2和H2O分子 |
| B、光照氯水,有气体逸出,该气体为Cl2 |
| C、新制氯水可使蓝色石蕊试纸先变红后褪色 |
| D、氯水密封放置数天后pH将变大 |
反应3A+B=2C+D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L?s);②v(B)=0.06mol/(L?s);③v(C)=0.05mol/(L?s);④v(D)=0.045mol/(L?s).则反应进行由快到慢的顺序为( )
①v(A)=0.15mol/(L?s);②v(B)=0.06mol/(L?s);③v(C)=0.05mol/(L?s);④v(D)=0.045mol/(L?s).则反应进行由快到慢的顺序为( )
| A、④>③>①>② |
| B、②>④>③>① |
| C、②>①>④>③ |
| D、④>③>②>① |
分析如图所示的四个装置,其中结论正确的是( )
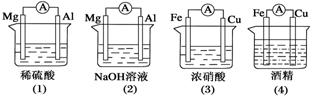

| A、(1)(2)中Mg作负极 |
| B、(3)中Fe作负极,电极反应为Fe-2e-═Fe2+ |
| C、(2)中Mg作正极,电极反应为6H2O+6e-═6OH-+3H2↑ |
| D、(4)中Fe作负极,电极反应为Fe-2e-═Fe2+ |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
| B、10mL pH=6的纯水中含有OH-离子数为10-10 NA |
| C、100 mL 1 mol?L-1 的Na2CO3溶液中含有CO32-离子数为0.1NA |
| D、14g由N2与CO组成的混合气体含有的原子数目为NA |

