题目内容
居室装修用石材的放射性常用
Ra作为标准,
Ra和
Ra是镭的两种同位素.下列有关Ra的说法正确的是( )
226 88 |
224 88 |
226 88 |
| A、镭的金属性比钙强,镭是第七周期Ⅱ族元素 | ||||
B、
| ||||
| C、镭单质能与水反应,放出氢气,生成的Ra(OH)2是一种两性氢氧化物 | ||||
D、Ra的碳酸盐难溶于水,
|
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.88226Ra(镭)质子数为88,则88-2-8-8-18-18-32=2,故处于Ra元素位于元素周期表第七周期ⅡA族,同主族自上而下金属性增强;
B.
Ra原子的质量数为226,中子数=质量数-质子数,进而计算中子数与核外电子数之差;
C.镭的金属性比Ca强;
D.根据碳酸镁、碳酸钙、碳酸钡溶解度推断Ra的碳酸盐溶解性,同位素原子化学性质几乎相同.
B.
226 88 |
C.镭的金属性比Ca强;
D.根据碳酸镁、碳酸钙、碳酸钡溶解度推断Ra的碳酸盐溶解性,同位素原子化学性质几乎相同.
解答:
解:A.同主族自上而下金属性增强,故镭的金属性比钙强,88226Ra(镭)质子数为88,则88-2-8-8-18-18-32=2,故处于Ra元素位于元素周期表第七周期ⅡA族,故A错误;
B.
Ra原子的质量数为226,中子数=226-88=138,中子数与核外电子数之差=138-88=50,其近似相对原子质量为226,故B错误;
C.镭的金属性比Ca强,则Ra(OH)2是一种强碱,故C错误;
D.碳酸镁微溶、碳酸钙、碳酸钡不溶,可推知Ra的碳酸盐难溶于水,
Ra和
Ra互为同位素原子,化学性质几乎相同,故D正确,
故选D.
B.
226 88 |
C.镭的金属性比Ca强,则Ra(OH)2是一种强碱,故C错误;
D.碳酸镁微溶、碳酸钙、碳酸钡不溶,可推知Ra的碳酸盐难溶于水,
224 88 |
226 88 |
故选D.
点评:本题考查结构性质位置关系应用,根据质子数确定元素在周期表中的位置是关键,注意掌握同主族元素化合物的相似性和递变性,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质熔化或升华时,所克服的粒子间作用属于同种类型的是( )
| A、NaCl和金刚石 |
| B、Si和Fe |
| C、CO2和SiO2 |
| D、碘和干冰升华 |
已知X、Y中含有相同的元素,Z、W中也含有相同的元素,根据反应X+H2O→Y+H2;Z+H2O→W+O2 (方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为( )
| A、X>Y、Z>W |
| B、X<Y、Z<W |
| C、X>Y、Z<W |
| D、X<Y、Z>W |
下列离子方程式书写正确的是( )
| A、向NH4HCO3溶液中加过量Ca(OH)2溶液:HCO3-+OH-+Ca2+═CaCO3↓+H2O | ||||
B、用惰性电极MgCl2电解水溶液:2Cl-+2H2O
| ||||
| C、向偏铝酸钠溶液中加入少量硫酸氢钠溶液:AlO2-+H++H2O═Al(OH)3↓ | ||||
| D、浓盐酸跟二氧化锰混合共热:MnO2+4H++4Cl-═MnO2++2H2O+2Cl2 |
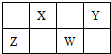
如图是元素周期表短周期的一部分,Y、W的质子数之和为25.下列说法正确的是( )

| A、非金属性:W>Z |
| B、原子半径:X<Y |
| C、Z的最高价氧化物可溶于Y的氢化物的水溶液 |
| D、Y的最高价氧化的水化物酸性强于W最高价氧化的水化物 |
某学生欲完成反应2HCl+2Ag═2AgCl↓+H2↑而设计了如图四个实验,你认为可行的是( )
A、 HCl |
B、 HCl |
C、 HCl |
D、 HCl |
金属的下列性质中,不能用金属的电子气理论加以解释的是( )
| A、易导电 | B、易导热 |
| C、不透明 | D、有延展性 |
下列说法正确的是( )
| A、HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 | ||||
| B、原子最外层电子数为2的元素一定处于元素周期表ⅡA族 | ||||
| C、第3周期元素的最高正化合价等于它所处的主族序数 | ||||
D、
|