题目内容
下列离子方程式书写正确的是( )
| A、向NH4HCO3溶液中加过量Ca(OH)2溶液:HCO3-+OH-+Ca2+═CaCO3↓+H2O | ||||
B、用惰性电极MgCl2电解水溶液:2Cl-+2H2O
| ||||
| C、向偏铝酸钠溶液中加入少量硫酸氢钠溶液:AlO2-+H++H2O═Al(OH)3↓ | ||||
| D、浓盐酸跟二氧化锰混合共热:MnO2+4H++4Cl-═MnO2++2H2O+2Cl2 |
考点:离子方程式的书写
专题:离子反应专题
分析:A、过量型离子方程式书写时,设量少的为“1”,根据量少的物质确定实际被消耗的过量的物质;
B、要考虑生成的OH-与Mg2+的反应;
C、考虑硫酸氢钠量的关系对反应的影响;
D、电荷不守恒.
B、要考虑生成的OH-与Mg2+的反应;
C、考虑硫酸氢钠量的关系对反应的影响;
D、电荷不守恒.
解答:
解:A、向NH4HCO3溶液中加过量Ca(OH)2溶液,设量少的NH4HCO3为1mol,则消耗2molOH-和1molCa2+,故离子方程式为NH4++HCO3-+2OH-+Ca2+═CaCO3↓+2H2O+NH3↑,故A错误;
B、用惰性电极MgCl2电解水溶液时,阳极上Cl-放电:2Cl--2e-=Cl2↑,阴极上来自于H2O的H+放电:2H2O+2e-=H2↑+2OH-,生成的OH-与Mg2+的反应生成Mg(OH)2沉淀,故离子方程式为:Mg2++2Cl-+2H2O
Cl2↑+H2↑+Mg(OH)2↓,故B错误;
C、NaHSO4在水溶液中完全电离:NaHSO4 =Na++H++SO42-,故向偏铝酸钠溶液中加入少量硫酸氢钠溶液时,AlO2-结合H+转化为Al(OH)3沉淀:AlO2-+H++H2O═Al(OH)3↓,故C正确;
D、浓盐酸跟二氧化锰混合共热的化学方程式:MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑,离子方程式为:MnO2+4H++4Cl-
Mn2++2H2O+Cl2↑,故D错误.
故选C.
B、用惰性电极MgCl2电解水溶液时,阳极上Cl-放电:2Cl--2e-=Cl2↑,阴极上来自于H2O的H+放电:2H2O+2e-=H2↑+2OH-,生成的OH-与Mg2+的反应生成Mg(OH)2沉淀,故离子方程式为:Mg2++2Cl-+2H2O
| ||
C、NaHSO4在水溶液中完全电离:NaHSO4 =Na++H++SO42-,故向偏铝酸钠溶液中加入少量硫酸氢钠溶液时,AlO2-结合H+转化为Al(OH)3沉淀:AlO2-+H++H2O═Al(OH)3↓,故C正确;
D、浓盐酸跟二氧化锰混合共热的化学方程式:MnO2+4HCl(浓)
| ||
| ||
故选C.
点评:本题考查了与量有关的离子方程式的书写和电解反应离子方程式的书写,难度较大,掌握方法是关键.

练习册系列答案
相关题目
关于原子结构、元素性质的说法正确的是( )
| A、随原子序数的递增,元素原子的核外电子数增多,原子半径逐渐减小 |
| B、若两种不同的核素具有相同的中子数,则二者一定不属于同种元素 |
| C、Si、P、S、Cl 相应的氧化物对应水化物的酸性依次增强 |
| D、在元素周期表中,各主族元素的最高化合价与其族序数相等 |
由几种常见的盐混合组成的白色粉末,其中只可能含有Na+、K+、Al3+、CO32-、HCO3-、SO42-、NO2-中的若干种离子.某同学对该溶液进行如图实验,以下说法正确的是( )


| A、白色沉淀甲是Al(OH)3,气体甲是CO2,所以混合物一定含Al3+和HCO3- |
| B、气体乙一定是NO和NO2的混合气体 |
| C、白色沉淀乙是BaSO4,所以原混合物一定含有SO42- |
| D、白色粉末中一定含有Na+、Al3+、NO2- |
 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图.下列说法正确的是( )
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图.下列说法正确的是( )| A、a为CH4,b为CO2 |
| B、CO32-向正极移动 |
| C、此电池在常温时也能工作 |
| D、正极反应式为:O2+2CO2+4e-═2CO32- |
居室装修用石材的放射性常用
Ra作为标准,
Ra和
Ra是镭的两种同位素.下列有关Ra的说法正确的是( )
226 88 |
224 88 |
226 88 |
| A、镭的金属性比钙强,镭是第七周期Ⅱ族元素 | ||||
B、
| ||||
| C、镭单质能与水反应,放出氢气,生成的Ra(OH)2是一种两性氢氧化物 | ||||
D、Ra的碳酸盐难溶于水,
|
在①浓硝酸 ②氧气 ③浓硫酸 ④氢氟酸 ⑤氢氧化钾溶液中,能与单质硅起化学反应的是( )
| A、①②④ | B、②④⑤ |
| C、③④⑤ | D、③④ |
有关实验的描述中,下列叙述正确的是( )
①钠放入水中后,沉在水下缓缓冒出气体
②Na2CO3和NaHCO3的溶液都可以使无色酚酞试液变红
③将某气体通入品红溶液中,红色褪去,说明该气体一定是SO2
④向某溶液中加入烧碱溶液,加热后生成使湿润的红色石蕊试纸变蓝的气体,说明原溶液中有NH4+
⑤除去NaCl中混有的少量KNO3.采用蒸发结晶,趁热过滤的方法.
①钠放入水中后,沉在水下缓缓冒出气体
②Na2CO3和NaHCO3的溶液都可以使无色酚酞试液变红
③将某气体通入品红溶液中,红色褪去,说明该气体一定是SO2
④向某溶液中加入烧碱溶液,加热后生成使湿润的红色石蕊试纸变蓝的气体,说明原溶液中有NH4+
⑤除去NaCl中混有的少量KNO3.采用蒸发结晶,趁热过滤的方法.
| A、①④⑤ | B、②④⑤ |
| C、②③④ | D、③④⑤ |
按碳的骨架进行分类,下列各物质中与其他三种不属于同一类的是( )
| A、乙炔 | B、乙烯 | C、戊烷 | D、苯 |
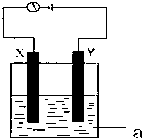 (1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是