题目内容
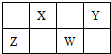
如图是元素周期表短周期的一部分,Y、W的质子数之和为25.下列说法正确的是( )

| A、非金属性:W>Z |
| B、原子半径:X<Y |
| C、Z的最高价氧化物可溶于Y的氢化物的水溶液 |
| D、Y的最高价氧化的水化物酸性强于W最高价氧化的水化物 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由短周期元素在周期表中的位置,可知X、Y处于第二周期,Z、W处于第三周期,令Y的质子数为a,则W质子数为a+7,Y、W的质子数之和为25,则a+a+7=25,解得a=9,故Y为F元素,可推知X为N元素、Z为Si、W为S元素,
A.同周期自左而右元素非金属性增强;
B.同周期自左而右原子半径减小;
C.二氧化硅与HF反应生成四氟化硅与水;
D.氟元素没有最高价含氧酸.
A.同周期自左而右元素非金属性增强;
B.同周期自左而右原子半径减小;
C.二氧化硅与HF反应生成四氟化硅与水;
D.氟元素没有最高价含氧酸.
解答:
解:由短周期元素在周期表中的位置,可知X、Y处于第二周期,Z、W处于第三周期,令Y的质子数为a,则W质子数为a+7,Y、W的质子数之和为25,则a+a+7=25,解得a=9,故Y为F元素,可推知X为N元素、Z为Si、W为S元素,
A.同周期自左而右元素非金属性增强,故非金属性:W>Z,故A正确;
B.同周期自左而右原子半径减小,故原子半径:X>Y,故B错误;
C.二氧化硅与HF反应生成四氟化硅与水,故C正确;
D.氟元素没有最高价含氧酸,故D错误,
故选AC.
A.同周期自左而右元素非金属性增强,故非金属性:W>Z,故A正确;
B.同周期自左而右原子半径减小,故原子半径:X>Y,故B错误;
C.二氧化硅与HF反应生成四氟化硅与水,故C正确;
D.氟元素没有最高价含氧酸,故D错误,
故选AC.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,D选项为易错点,学生容易根据非金属性强弱判断,忽略氟元素没有最高价含氧酸,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下表为部分短周期元素的原子半径及主要化合价.下列说法正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +3 | +6,-2 | +5,-3 | -2 |
| A、气态氢化物的稳定性:R>T |
| B、工业上电解MCl3溶液制备单质M |
| C、化合物L2T与QT2所含化学键类型相同 |
| D、L与Q的最高价氧化物的水化物均能与M(OH)3反应 |
下列说法中正确的是( )
| A、工业上通过设法除去乙醇和氢氧化钠的作用生成的水来制取乙醇钠 |
| B、只使用试管和胶头滴管即可鉴别NaNO2、NaCl、AgNO3、H2SO4四种无色溶液 |
| C、将燃烧的镁条伸入混合气体,以除去CO2中的N2 |
| D、用硫酸镁和硫酸亚铁混合溶液制摩尔盐的过程:蒸发浓缩→冷却结晶→抽滤→用水洗涤2-3次 |
居室装修用石材的放射性常用
Ra作为标准,
Ra和
Ra是镭的两种同位素.下列有关Ra的说法正确的是( )
226 88 |
224 88 |
226 88 |
| A、镭的金属性比钙强,镭是第七周期Ⅱ族元素 | ||||
B、
| ||||
| C、镭单质能与水反应,放出氢气,生成的Ra(OH)2是一种两性氢氧化物 | ||||
D、Ra的碳酸盐难溶于水,
|
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、c(ClO-)=1.0 mol?L-1的溶液中:Na+、SO32-、S2-、SO42- | ||
B、常温下,
| ||
| C、由水电离的c(H+)=1×10-12 mol?L-1的溶液中:Ba2+、K+、Cl-、NO3- | ||
| D、滴入少量KSCN溶液显红色的溶液中:Na+、K+、I-、SO42- |
下列物质属于弱电解质的是( )
| A、HNO3 |
| B、NaOH |
| C、KCl |
| D、CH3COOH |
塑化剂DEHP的作用类似于人工荷尔蒙,会危害男性生殖能力并促使女性性早熟,长期大量摄取会导致肝癌.其毒性远高于三聚氰胺,会造成免疫力及生殖力下降.下列关于塑化剂邻苯二甲酸二正丁酯说法不正确的是( )
| A、分子式为C16H22O4,可由石油化工原料通过取代,氧化,酯化反应制得 |
| B、白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去 |
| C、用核磁共振氢谱分析有6个吸收峰 |
| D、邻苯二甲酸二正丁酯能发生加成,取代和氧化反应 |
 某含碳、氢、氧的有机物A能发生如图所示的变化:已知A、C、D、E均能在一定条件下与新制的氢氧化铜悬浊液反应生成红色沉淀,则A的同分异构体是( )
某含碳、氢、氧的有机物A能发生如图所示的变化:已知A、C、D、E均能在一定条件下与新制的氢氧化铜悬浊液反应生成红色沉淀,则A的同分异构体是( )| A、乙酸 | B、甲酸乙酯 |
| C、甲酸甲酯 | D、乙酸甲酯 |