题目内容
将两个铂电极插入500mL CuSO4溶液中进行电解,通电一段时间后,某一电极增重0.032g(电解时无氢气放出,不考虑水解和溶液体积变化),此时溶液中H+的浓度约为( )
| A、4×10-3mol?L-1 |
| B、2×10-3mol?L-1 |
| C、1×10-3mol?L-1 |
| D、1×10-7mol?L-1 |
考点:电解原理
专题:电化学专题
分析:电解CuSO4溶液质量增重的一极是电解池的阴极,析出铜,根据电解方程式计算,电解方程式为:2CuSO4+2H20
2Cu+2H2SO4+O2↑,也可根据电解池两极上转移的电子数目相等计算,利用关系式为Cu~2e-~2H+来解答.
| ||
解答:
解:设生成硫酸的物质的量为x,
2CuSO4+2H20
2Cu+2H2SO4+O2↑
128g 2mol
0.032g x
x=
=0.0005mol
n(H+)=0.0005mol×2=0.001mol
c(H+)=
=2×10-3mol/L
故选B.
2CuSO4+2H20
| ||
128g 2mol
0.032g x
x=
| 0.032mol×2 |
| 128g |
n(H+)=0.0005mol×2=0.001mol
c(H+)=
| 0.001mol |
| 0.5L |
故选B.
点评:本题考查电解原理,计算本题时可根据化学方程式就算,也可根据电解池两极上转移的电子数目相等计算,题目难度不大.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案
相关题目
下列化学用语表达正确的是( )
A、乙酸的分子比例模型图为: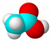 |
B、Mg原子结构示意图: |
| C、次氯酸的结构式为:H-Cl-O |
| D、丙烯的结构简式:CH3CH2CH |
ag铁粉与含有H2SO4的CuSO4溶液完全反应后,固体质量与反应前相同,则参加反应的CuSO4与H2SO4的物质的量之比为( )
| A、1:7 | B、7:1 |
| C、7:8 | D、8:7 |
“善待地球,科学发展,构建和谐”是“世界地球日”的主题.你认为下列行为不符的( )
| A、控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源 |
| B、研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展 |
| C、开发太阳能、水能、风能、可燃冰等新能源、减少使用煤、石油等化石燃料 |
| D、实现资源的“3R”利用,即:减少资源消耗、增加资源的重复使用、资源的循环利用 |
用铂电极分别电解下列各盐的水溶液,当消耗相同电量时,在阴极上析出的金属质量最大且溶液pH减小的是( )
| A、CuCl2 |
| B、KCl |
| C、CuSO4 |
| D、Al(NO3)3 |
0.1mol?L-1BaCl2溶液1000mL和0.8mol?L-1AgNO3溶液100mL充分混合后又加入0.06mol?L-1 ZnSO4溶液1000mL,最后溶液中浓度最大的离子是( )
| A、Ba2+ |
| B、Cl- |
| C、Ag+ |
| D、NO3- |
可逆反应①X(g)+2Y(g)?2Z(g)、②2M(g)?N(g)+p(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板.反应开始和达到平衡状态是有关物理量的变化如图所示:
下列判断正确的是( )

下列判断正确的是( )
| A、反应①的正反应是吸热反应 | ||
| B、在平衡(I)和平衡(II)中的气体摩尔体积相同 | ||
C、达平衡(I)是X的体积分数为
| ||
| D、达平衡(I)时体系的压强与反应开始时体系的压强之比为10:11 |
