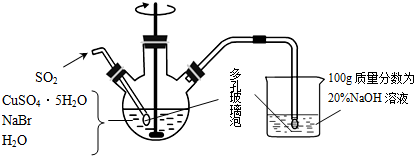
��Ŀ����
10��Cl2���仯�����������������о��й㷺����;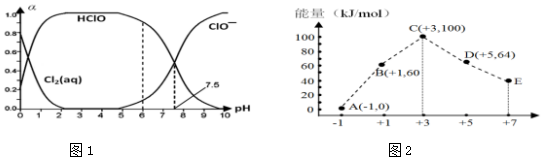
��1��25��ʱ����������ˮ�γ�����-��ˮ��ϵ������ϵ��Cl2��aq����HClO��ClO-�ֱ�����������ռ������������pH�仯�Ĺ�ϵ��ͼ1��ʾ��
����֪HClO��ɱ��������ClO-ǿ����ͼ��������������������ˮʱ��pH=7.5�� pH=6ʱɱ��Ч��ǿ����pH=6ʱ��
������-��ˮ��ϵ�У����ڶ������Ԫ�ص�ƽ���ϵ���ֱ���ƽ�ⷽ��ʽ��ʾΪCl2��aq��+H2O?HClO+H++Cl-����HClO?H++ClO-��Cl2��g��?Cl2��aq��
��2��ClO2��һ���µ�����������ҵ�Ͽ���Cl2����NaClO2��Һ��ȡClO2��д���÷�Ӧ�Ļ�ѧ����ʽCl2+2NaClO2=2NaCl+2ClO2��
��3����ҵ�ϻ��������з����Ʊ�ClO2����80��ʱ����Ȼ�����Һ�õ�NaClO3��Ȼ�������ᷴӦ�õ�ClO2�����ʱ��NaClO3���������������������ɣ�����ClO3-�ĵ缫��ӦʽΪCl--6e-+3 H2O=6H++ClO3-��
��4��һ�������£���ˮ��Һ�� 1mol Cl-��1mol ClOx-��x=1��2��3��4����������С�뻯�ϼ۵Ĺ�ϵ��ͼ16-2��ʾ
�ٴ������Ƕȿ���C��D��E����ȶ���������ClO2-�������ӷ��ţ���
��B��A+D��Ӧ���Ȼ�ѧ����ʽΪ3ClO-��aq��=ClO3-��aq��+2Cl-��aq����H=-117kJ/mol�������ӷ��ű�ʾ����
���� ��1����HClO��ɱ��������ClO-ǿ������HClO��Ũ��Խ����ɱ��Ч��Խ�ã�
������ͼ�������֪�����ȵ����ʴ���ƽ���״̬Ϊ������ˮ��Ӧ�����������ƽ�⣬Һ̬��������̬������ƽ��ȣ�
��2��ClO2��һ���µ�����������ҵ�Ͽ���Cl2����NaClO2��Һ��ȡClO2�����ԭ���غ�͵����غ�д���÷�Ӧ�Ļ�ѧ���̣�
��3����ҵ�ϻ��������з����Ʊ�ClO2����80��ʱ����Ȼ�����Һ�õ�NaClO3��������ʧ����������������������ӣ�
��4��������Խ��Խ���÷�����
��B��A+C������ת�Ƶ����غ�ø÷�Ӧ����ʽΪ3ClO-=ClO3-+2Cl-����Ӧ��=��62kJ/mol+2��0kJ/mol��-3��60kJ/mol=-116kJ/mol��
��� �⣺��1������ɱ�����õ���HClO����ͼ���֪��pH=6.5ʱc��HClO����pH=7.5ʱҪ��HClOŨ��Խ��ɱ��Ч���ã�����pH=7.5ʱɱ��Ч����pH=6.5ʱ�
�ʴ�Ϊ��pH=6ʱ��
�ں��ȵ����ʴ���ƽ���״̬Ϊ������ˮ��Ӧ�����������ƽ�⣬Һ̬��������̬������ƽ��ȣ�����-��ˮ��ϵ�У����ڶ������Ԫ�ص�ƽ���ϵ���ֱ���ƽ�ⷽ��ʽ��ʾΪCl2��aq��+H2O?HClO+H++Cl-�� HClO?H++ClO-��Cl2��g��?Cl2��aq����
�ʴ�Ϊ��Cl2��aq��+H2O?HClO+H++Cl-��HClO?H++ClO-��Cl2��g��?Cl2��aq����
��2��ClO2��һ���µ�����������ҵ�Ͽ���Cl2����NaClO2��Һ��ȡClO2�����ԭ���غ�͵����غ�д���÷�Ӧ�Ļ�ѧ����Cl2+2NaClO2=2NaCl+2ClO2��
�ʴ�Ϊ��Cl2+2NaClO2=2NaCl+2ClO2��
��3����ҵ�ϻ��������з����Ʊ�ClO2����80��ʱ����Ȼ�����Һ�õ�NaClO3��������ʧ����������������������ӣ��缫��ӦΪ��Cl--6e-+3 H2O=6H++ClO3-��
�ʴ�Ϊ������ Cl--6e-+3 H2O=6H++ClO3-��
��4����ͼ�������֪������Խ��Խ���ã�+3�۵����������ΪClO2-��
�ʴ�Ϊ��ClO2-��
��B��A+C������ת�Ƶ����غ�ø÷�Ӧ����ʽΪ3ClO-=ClO3-+2Cl-����Ӧ��=��62kJ/mol+2��0kJ/mol��-3��60kJ/mol=-116kJ/mol�����Ը��Ȼ�ѧ��Ӧ����ʽΪ3ClO-��aq��=ClO3-��aq��+2Cl-��aq����H=-116kJ/mol��
�ʴ�Ϊ��3ClO-��aq��=ClO3-��aq��+2Cl-��aq����H=-117kJ/mol��
���� ��������ˮΪ���忼���˻�ѧƽ�ⳣ���ļ��㡢���ʵ��ȶ��Ե�֪ʶ�㣬��ȷ����ͼ���и����������Ĺ�ϵ�ǽⱾ��ؼ����ٽ�ϸ�˹���ɡ����ʵ����ʵ�֪ʶ�������������Ŀ�Ѷ��еȣ�

 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д� Ӣ�żƻ���ĩ����ϵ�д�
Ӣ�żƻ���ĩ����ϵ�д�| A�� | �٢ڢۢ� | B�� | �ڢۢܢ� | C�� | �ڢ٢ۢ� | D�� | �ܢڢۢ� |
| A�� | ��ˮϡ�ͺ���Һ��$\frac{c��N{H}_{4}^{+}��}{c��N{H}_{3}•{H}_{2}O��}$��ֵ��С | |
| B�� | 0.1 mol•L-1Na2CO3��Һ������ˮϡ�ͣ�CO32-��ˮ��̶�������Һ��pH��С | |
| C�� | ��⾫��ͭ�����У����������ļ�������������������һ����� | |
| D�� | 298 Kʱ��2H2S��g��+SO2��g���T3S��s��+2H2O��l�����Է����У������H��0 |
| A�� | 142g�����к�Cl2�ķ�����Ϊ2NA | |
| B�� | 1.7gOH-���������ӵ���ĿΪNA | |
| C�� | 49g������������ԭ�ӵ���ĿΪ2NA | |
| D�� | 71g�����������������ӵ���ĿΪ2NA |
| A�� | ���þ�����ϩ������ϩ����ʳƷ��װ�� | |
| B�� | ȥ����������Ag2S���ɽ���������ʢ��ʳ�����������Ƭ�� | |
| C�� | �������ܡ�̫���ܵ�����Դ���ƹ�״����ͣ�ʹ������ϴ�Ӽ������ϻ������� | |
| D�� | ��������ά���͡����ղ�����Ҫ����̼���衢�մɺ�̼��ά���϶��ɣ���һ���������ǽ������� |
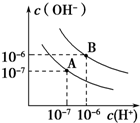 ��֪ˮ��25���95��ʱ�������ƽ��������ͼ��ʾ��
��֪ˮ��25���95��ʱ�������ƽ��������ͼ��ʾ��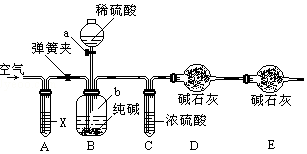 ij������Ʒ�к��������Ȼ������ʣ�������ͼ��ʾװ�����ⶨ������Ʒ��̼���Ƶ���������������̨�����е���ͼ�о�����ȥ����ʵ�鲽�����£�
ij������Ʒ�к��������Ȼ������ʣ�������ͼ��ʾװ�����ⶨ������Ʒ��̼���Ƶ���������������̨�����е���ͼ�о�����ȥ����ʵ�鲽�����£�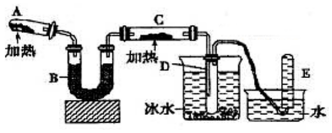 ��֪�����������ȵ�����ͭ��Ӧ�õ������ͽ���ͭ����ʾ��ͼ�е�װ�ÿ���ʵ�ָ÷�Ӧ��
��֪�����������ȵ�����ͭ��Ӧ�õ������ͽ���ͭ����ʾ��ͼ�е�װ�ÿ���ʵ�ָ÷�Ӧ��