题目内容
学校化学研究小组对某溶液进行检测分析,该无色溶液中可能含有NH4+、K+、Al3+、HCO3-、Cl-、MnO4-、SO42-等离子中的几种离子.
①经实验可知溶液明显呈酸性.
②取10mL该溶液于试管中滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲,向滤液中加入AgNO3溶液未见沉淀产生.
③另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解.
(1)写出气体丙的电子式 .
(2)该溶液中一定不含有: (填离子的化学式)离子,一定含有的离子有 (填离子的化学式).
(3)在这些不存在的离子中,有一种离子在酸性环境中与SO2反应,试写出该反应的离子方程式 .
(4)请设计实验方案,检验该试液中是否存在可能含有的离子 .
①经实验可知溶液明显呈酸性.
②取10mL该溶液于试管中滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲,向滤液中加入AgNO3溶液未见沉淀产生.
③另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解.
(1)写出气体丙的电子式
(2)该溶液中一定不含有:
(3)在这些不存在的离子中,有一种离子在酸性环境中与SO2反应,试写出该反应的离子方程式
(4)请设计实验方案,检验该试液中是否存在可能含有的离子
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:溶液无色,说明不含MnO4-;
①经实验可知溶液明显呈酸性,可为强酸弱碱盐,则一定不存在水解呈碱性的HCO3-离子;
②取10mL该溶液于试管中滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲,向滤液中加入AgNO3溶液未见沉淀产生,说明含有SO42-,不含有Cl-,
甲为BaSO4;
③另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解,说明含有NH4+、Al3+,乙为Al(OH)3,
丙为NH3,K+应通过焰色反应检验.
①经实验可知溶液明显呈酸性,可为强酸弱碱盐,则一定不存在水解呈碱性的HCO3-离子;
②取10mL该溶液于试管中滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲,向滤液中加入AgNO3溶液未见沉淀产生,说明含有SO42-,不含有Cl-,
甲为BaSO4;
③另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解,说明含有NH4+、Al3+,乙为Al(OH)3,
丙为NH3,K+应通过焰色反应检验.
解答:
解:溶液无色,说明不含MnO4-;
①经实验可知溶液明显呈酸性,可为强酸弱碱盐,则一定不存在水解呈碱性的HCO3-离子;
②取10mL该溶液于试管中滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲,向滤液中加入AgNO3溶液未见沉淀产生,说明含有SO42-,不含有Cl-,
甲为BaSO4;
③另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解,说明含有NH4+、Al3+,乙为Al(OH)3,
丙为NH3,
(1)由以上分析可知丙为NH3,电子式为 ,故答案为:
,故答案为: ;
;
(2)由以上分析可知一定含有的离子为NH4+、Al3+、SO42-,一定不含有的离子为MnO4-、HCO3-、Cl-,
故答案为:MnO4-、HCO3-、Cl-;NH4+、Al3+、SO42-;
(3)能与二氧化硫反应的离子应具有强氧化性,应为MnO4-,反应的离子方程式为2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+,
故答案为:2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+;
(4)K+应通过焰色反应检验,实验方法是用洁净的铂丝蘸取试样在无色火焰上灼烧,透过蓝色钴玻璃,观察火焰颜色,若紫色,则含有K+,
故答案为:焰色反应,用洁净的铂丝蘸取试样在无色火焰上灼烧,透过蓝色钴玻璃,观察火焰颜色,若紫色,则含有K+.
①经实验可知溶液明显呈酸性,可为强酸弱碱盐,则一定不存在水解呈碱性的HCO3-离子;
②取10mL该溶液于试管中滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲,向滤液中加入AgNO3溶液未见沉淀产生,说明含有SO42-,不含有Cl-,
甲为BaSO4;
③另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解,说明含有NH4+、Al3+,乙为Al(OH)3,
丙为NH3,
(1)由以上分析可知丙为NH3,电子式为
 ,故答案为:
,故答案为: ;
;(2)由以上分析可知一定含有的离子为NH4+、Al3+、SO42-,一定不含有的离子为MnO4-、HCO3-、Cl-,
故答案为:MnO4-、HCO3-、Cl-;NH4+、Al3+、SO42-;
(3)能与二氧化硫反应的离子应具有强氧化性,应为MnO4-,反应的离子方程式为2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+,
故答案为:2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+;
(4)K+应通过焰色反应检验,实验方法是用洁净的铂丝蘸取试样在无色火焰上灼烧,透过蓝色钴玻璃,观察火焰颜色,若紫色,则含有K+,
故答案为:焰色反应,用洁净的铂丝蘸取试样在无色火焰上灼烧,透过蓝色钴玻璃,观察火焰颜色,若紫色,则含有K+.
点评:本题主要考查未知物的判断以及含量的测定,题目难度较大,注意根据实验现象判断可能含有的离子,把握溶液电荷守恒的运用.

练习册系列答案
相关题目
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应 2X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A、反应前2min的平均速率ν(Z)=0.04mol?L-1?min-1 |
| B、其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正) |
| C、该温度下此反应的平衡常数K=90L/mol |
| D、其他条件不变,再充入0.2molZ,平衡时X的体积分数减小 |
电子在原子核外排布时,必须遵循的原则是( )
①电子排布在同一能级时,总是优先单独占据不同轨道,且自旋方向相同
②电子排布在不同能级时,总是优先占据能量低的轨道,然后再占据能量高的轨道
③电子排布在同一轨道时,最多只能排2个,且自旋方向必须相反
④电子的排布总是遵循“能量最低原理”“泡利不相容原理”和“洪特规则”
①电子排布在同一能级时,总是优先单独占据不同轨道,且自旋方向相同
②电子排布在不同能级时,总是优先占据能量低的轨道,然后再占据能量高的轨道
③电子排布在同一轨道时,最多只能排2个,且自旋方向必须相反
④电子的排布总是遵循“能量最低原理”“泡利不相容原理”和“洪特规则”
| A、①② | B、②④ | C、①③ | D、②③④ |
下列分子中所有原子都满足最外层8电子结构的是( )
| A、NH3 |
| B、PCl5 |
| C、COCl2 |
| D、BF3 |
下列元素的最外层电子数为5的是( )
| A、H | B、Li | C、Na | D、P |
胡妥油(D)用作香料的原料,它可由A合成得到:则下列说法正确的是( )
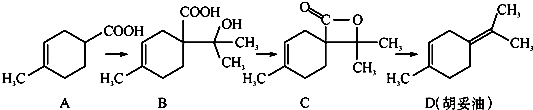

| A、若A是由异戊二烯(C5H8)和丙烯酸(C3H4O2)加热得到的,则该反应的属于加成反应 |
| B、有机物B既能跟Na反应放出H2,又能跟NaHCO3溶液反应放出CO2气体 |
| C、有机物C的所有同分异构体中不可能有芳香族化合物存在 |
| D、有机物D分子中所有碳原子不一定共面 |
 现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子X、Cl-、OH-、NO3-、CO32-中的一种.
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子X、Cl-、OH-、NO3-、CO32-中的一种.