题目内容
下列分子中含有σ键的是共价化合物是( )
| A、F2 |
| B、金刚石 |
| C、Na2O |
| D、NH3 |
考点:共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:共价键中,单键为σ键,双键和三键中含1个σ键,结合化合物由至少两种元素组成来解答.
解答:
解:A.F2为单质,含σ键,故A不选;
B.金刚石为碳的单质,含σ键,故B不选;
C.Na2O为含离子键的离子化合物,故C不选;
D.NH3为只含N-H共价键的共价化合物,含σ键,故D选;
故选D.
B.金刚石为碳的单质,含σ键,故B不选;
C.Na2O为含离子键的离子化合物,故C不选;
D.NH3为只含N-H共价键的共价化合物,含σ键,故D选;
故选D.
点评:本题考查共价键和共价化合物,为高频考点,把握共价化合物的判断为解答的关键,侧重共价键类型及物质分类考查,题目难度不大.

练习册系列答案
相关题目
下列物质中,能够导电,但不属于电解质的是( )
| A、NaOH固体 | B、稀盐酸 |
| C、熔化的NaCl | D、蔗糖 |
氧化还原反应在生产生活中具有广泛的用途.下列事实不涉及氧化还原反应的是( )
| A、食物腐败 |
| B、点制豆腐 |
| C、金属锈蚀 |
| D、久置氢氧化钠会变质 |
四个电解装置都以Pt作电极,它们分别装着如下电解质溶液进行电解,电解一段时间后,测定其pH变化,所记录的结果正确的是( )
| A | B | C | D | |
| 电解质溶液 | HCl | AgNO3 | KOH | BaCl2 |
| pH变化 | 减小 | 增大 | 增大 | 不变 |
| A、A | B、B | C、C | D、D |
下列说法正确的是( )
| A、物质失去电子数越多,物质的还原性越强 |
| B、导电的不一定是电解质,电解质不一定导电 |
| C、得到电子的物质是还原剂 |
| D、还原剂反应后得到是还原产物 |
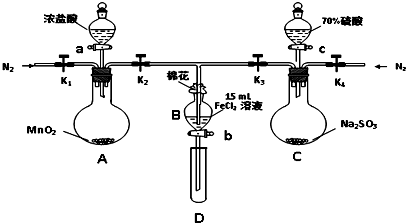
 某学校化学学习小组为探究二氧化氮的性质,按图所示装置进行实验.请回答下列问题
某学校化学学习小组为探究二氧化氮的性质,按图所示装置进行实验.请回答下列问题