题目内容
1.下列物质的水溶液能导电,但属于非电解质的是( )| A. | Na2S | B. | CH3CH2 OH | C. | NaHCO3 | D. | SO2 |
分析 电解质是指在水溶液或熔化状态下能导电的化合物,而非电解质是指在水溶液和熔化状态下都不能导电的化合物,据此进行判断.
解答 解:A.硫化钠在溶液中能够电离出钠离子和硫离子,溶液导电,硫化钠属于电解质,故A错误;
B.乙醇其水溶液不导电是非电解质,故B错误;
C.碳酸氢钠溶液能够导电,碳酸氢钠属于电解质,能够电离出钠离子和碳酸氢根离子,故C错误;
D.二氧化硫溶于水生成亚硫酸,亚硫酸是电解质,电离出离子使能够导电,但是溶液导电的原因不是二氧化硫电离的离子,所以二氧化硫不属于电解质,属于非电解质,水溶液能导电,故D正确;
故选D.
点评 本题考查电解质和非电解质,学生应明确电解质和非电解质都是化合物,并明确判断电解质时发生电离的为化合物本身来分析解答即可,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列情境中,对分离原理说法错误的是( )
| A. | 沙里淘金,利用了沙子和金子的密度不同 | |
| B. | 海水晒盐,利用了水和NaCl的沸点不同 | |
| C. | 酒糟酿酒,利用了粮食和酒精分子的颗粒大小不同 | |
| D. | 植物油能萃取蔬菜汁中的植物精华--维生素,利用了维生素在水和油中溶解度不同 |
12.在标准状况下,相同质量的下列气体体积最小的是( )
| A. | O2 | B. | CO2 | C. | H2 | D. | SO2 |
16.下列叙述I和II均正确并有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | KNO3的溶解度大 | 用重结晶法除去KNO3中混有的NaCl |
| B | 收集铜与浓硝酸反应生成的气体,用冰水混合物冷却降温,气体颜色变浅 | 生成的红棕色NO2气体部分转化为无色气体 |
| C | 用pH试纸测定NaClO溶液的酸碱性,试纸显蓝色 | NaClO水解显碱性 |
| D | Ca(OH)2能制成澄清石灰水 | 可配制2.0mol•L-1的Ca(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
6.下列有关物质用途的说法中,不正确的是( )
| A. | 氯气可做自来水消毒剂 | B. | 碳酸钠可用于制造玻璃制造肥皂 | ||
| C. | 二氧化硅可用于制造集成电路 | D. | Na2O2用作潜水艇供氧剂 |
13.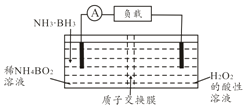 直接氨硼烷(NH3•BH3)电池可在常温下工作,装置如下图,该电池的总反应为NH3•BH3+3H2O2═NH4BO2+4H2O.下列说法正确的是( )
直接氨硼烷(NH3•BH3)电池可在常温下工作,装置如下图,该电池的总反应为NH3•BH3+3H2O2═NH4BO2+4H2O.下列说法正确的是( )
 直接氨硼烷(NH3•BH3)电池可在常温下工作,装置如下图,该电池的总反应为NH3•BH3+3H2O2═NH4BO2+4H2O.下列说法正确的是( )
直接氨硼烷(NH3•BH3)电池可在常温下工作,装置如下图,该电池的总反应为NH3•BH3+3H2O2═NH4BO2+4H2O.下列说法正确的是( )| A. | 左侧电极发生还原反应 | |
| B. | 电池工作时,H+通过质子交换膜向负极移动 | |
| C. | 正极的电极反应式为2H++2e-=H2↑ | |
| D. | 消耗3.1g氨硼烷,理论上转移0.6mol电子 |
10.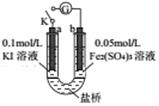 某同学用如图实验装置验证通过改变浓度来实现反应,2Fe3++2I-═2Fe2++I2中Fe3+与Fe2+的相互转化.K 闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴油加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反.下列有关说法不正确的是( )
某同学用如图实验装置验证通过改变浓度来实现反应,2Fe3++2I-═2Fe2++I2中Fe3+与Fe2+的相互转化.K 闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴油加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反.下列有关说法不正确的是( )
 某同学用如图实验装置验证通过改变浓度来实现反应,2Fe3++2I-═2Fe2++I2中Fe3+与Fe2+的相互转化.K 闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴油加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反.下列有关说法不正确的是( )
某同学用如图实验装置验证通过改变浓度来实现反应,2Fe3++2I-═2Fe2++I2中Fe3+与Fe2+的相互转化.K 闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴油加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反.下列有关说法不正确的是( )| A. | 指针第一次偏转时,b极反应式为Fe3++e-═Fe2+ | |
| B. | 加入AgNO3后,a为正极 | |
| C. | 当b极有0.001molFe3+被还原时,则通过盐桥的电子数为0.001NA | |
| D. | 第二次指针偏转的原因是:I-浓度减小,反应逆向进行 |
15.下列实验操作能达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将饱和的FeCl3溶液滴加到NaOH浓溶液中 |
| B | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干,趁热过滤 |
| C | 除去HBr中混有的Br2 | 将混合气通入盛有CCl4的洗气瓶 |
| D | 证明Cu(OH)2的溶度积比Mg(OH)2的小 | 将1mL0.1mol•L-1MgSO4溶液逐滴滴入4mL0.1mol•L-1NaOH溶液,再滴加1mL0.1mol•LCuSO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
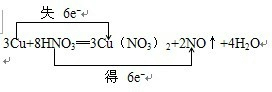 ,该反应中氧化剂是硝酸,氧化产物与还原产物的物质的量之比为3:2.
,该反应中氧化剂是硝酸,氧化产物与还原产物的物质的量之比为3:2.