题目内容
6.下列化学方程式中,能用离子方程式H++OH-→H2O表示的是( )| A. | 2H2+O2 $\stackrel{点燃}{→}$2H2O | B. | 2HCl+Ba(OH)2→2BaCl2+H2O | ||
| C. | H2SO4+Cu(OH)2→CuSO4+2H2O | D. | Ba(OH)2+H2SO4→BaSO4↓+2H2O |
分析 A.氢气与氧气的反应不是离子反应,无法书写离子方程式;
B.氢氧化钡和盐酸都是可溶性强酸,反应实质为氢离子与氢氧根离子生成水;
C.氢氧化铜为难溶物,离子方程式中不能拆开;
D.该反应充除了生成水,还生成了难溶物硫酸钡.
解答 解:A.反应2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O不是离子反应,无法书写离子方程式,故A错误;
B.2HCl+Ba(OH)2=2BaCl2+H2O的离子方程式为:H++OH-=H2O,故B正确;
C.H2SO4+Cu(OH)2=CuSO4+2H2O的离子方程式为:2H++Cu(OH)2=Cu2++2H2O,不能用H++OH-=H2O表示,故C错误;
D.Ba(OH)2+H2SO4=BaSO4↓+2H2O的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,不能用H++OH-=H2O表示,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度不大,明确离子方程式表示的意义为解答关键,注意掌握离子方程式的书写原则,试题有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
16.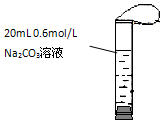 如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )
如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )
 如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )
如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )| A. | 有反应CO32-+2H+→CO2↑+H2O | |
| B. | 有反应CO32-+H+→HCO3-发生 | |
| C. | 有反应CO32-+CO2+H2O→2HCO3-发生 | |
| D. | 加快盐酸注入速度不会改变反应现象 |
17.化学与社会密切相关,下列说法正确的是( )
| A. | 硝铵与草木灰不能混合使用,否则将使前者失去肥效,而后者仍有肥效 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 可用于制作航天服的聚酯纤维是新型无机非金属材料 | |
| D. | 采用“静电除尘”、“原煤脱硫”、“汽车尾气催化净化”等方法,可提高空气质量 |
14.下列有关氧元素及化合物的表示正确的是( )
| A. | 中子数为10的氧原子:810O | B. | 氧负离子(O2-)的结构示意图: | ||
| C. | Na2O2的电子式: | D. | 1-丙醇的结构简式: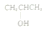 |
11.0.1mol/L某溶液的pH=5.1,该溶液中的溶质可能是下列的( )
| A. | HCl | B. | BaCl2 | C. | NaHSO4 | D. | NH4Cl |
18.下列各组离子是无色透明.并且在酸性条件时能大量共存的是( )
| A. | K+SO32-Cl- | B. | Cu2+SO42-NO3- | C. | Na+K+I- | D. | Ag+Br-Na+ |
15.下列变化中需要加入还原剂才能发生的是( )
| A. | N2→NO2 | B. | N2→NH3 | C. | NO→NO2 | D. | NH3→NO |
11.要确认集气瓶中是否收集满氯气,正确的操作是( )
| A. | 将AgNO3溶液滴入集气瓶中,观察是否生成白色沉淀 | |
| B. | 用手将湿润的淀粉碘化钾试纸放在集气瓶上方,观察试纸是否变蓝 | |
| C. | 将湿润的淀粉碘化钾试纸粘在玻棒一端,伸到集气瓶口,观察试纸是否变蓝 | |
| D. | 将紫色石蕊试液滴入集气瓶中,观察试液是否先变红后褪色 |