题目内容
19.下列各组反应(表中物质均为反应物),反应刚开始时,放出H2的速率最大的是( )| 编号 | 金属(粉末状)(mol) | 酸的浓度及体积 | 反应温度(℃) |
| A | Mg,0.1 | 6mol•L-1硝酸10mL | 60 |
| B | Mg,0.1 | 3mol•L-1盐酸10mL | 60 |
| C | Fe,0.1 | 3mol•L-1盐酸100mL | 60 |
| D | Mg,0.1 | 3mol•L-1硫酸5mL | 60 |
| A. | A | B. | B | C. | C | D. | D |
分析 影响化学反应速率的主要因素是物质的本身性质,对于同一个化学反应,反应物浓度越大,温度越高,反应速率越大,注意硝酸与金属反应不生成氢气.
解答 解:由金属的活泼性可知,Mg>Fe,则Mg与酸反应生成氢气的速率快,排除C,硝酸与金属反应不生成氢气,D中氢离子浓度最大,则反应速率最大.
故选D.
点评 本题考查化学反应速率的影响因素,难度不大,注意金属的活泼性强弱为影响反应速率的主要因素,易错点为A,注意硝酸与金属反应不生成氢气.

练习册系列答案
相关题目
9.下列化合物中不含离子键的是( )
| A. | (NH4+)2S | B. | Al2(SO4)3 | C. | KOH | D. | HNO3 |
10.X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增.X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14.下列说法正确的是( )
| A. | 原子半径由小到大的顺序:X<Y<Z<W | |
| B. | Z的最高价氧化物能与水反应生成相应的酸 | |
| C. | 室温下,0.1 mol/L W的气态氢化物的水溶液的pH>1 | |
| D. | Y单质在一定条件下可以与氧化铁发生置换反应 |
14.下列气体中,能使品红溶液褪色的是( )
| A. | N2 | B. | CO2 | C. | SO2 | D. | CH4 |
11.下列有关金属的说法正确的是( )
| A. | 湿法炼铜和火法炼铜的反应中,铜元素都发生还原反应 | |
| B. | 加强热,使CuO在高温条件下分解制备单质Cu | |
| C. | 黑色金属材料包括铁、铬、锰及其化合物 | |
| D. | 生铁与钢的区别在于生铁含碳杂质,而钢不含 |
8.可逆反应:N2(g)+3H2(g)?2NH3(g)的正逆反应速率可用反应物或生成物的浓度变化来表示,下列各关系中能说明反应已达平衡状态的是( )
| A. | v正(N2)=v正(H2) | B. | v正(N2)=v逆(NH3) | ||
| C. | 2 v正(H2)=3 v逆(NH3) | D. | v正(N2)=v逆(H2) |
18.NA为阿伏加德罗常数,下列叙述错误的是( )
| A. | 28 g C2H4和C4H8混合气体中含有氢原子总数为4NA | |
| B. | 常温常压下,Cu-Zn原电池中,正极产生1.12 L H2时,转移的电子数应小于0.1NA | |
| C. | 15g 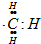 含有的电子数为9NA 含有的电子数为9NA | |
| D. | 2.1 g DTO中所含中子数为NA |
 现有下列四种物质,①H2②Cl2③SO2④H2SO4请回答相关问题:
现有下列四种物质,①H2②Cl2③SO2④H2SO4请回答相关问题: