题目内容
6.碳和氮的化合物与人类生产、生活密切相关.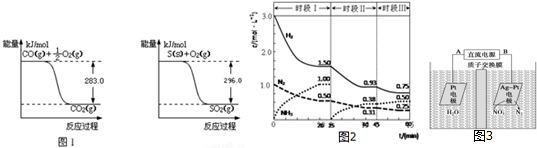
(1)C、CO、CO2在实际生产中有如下应用:
a.2C+SiO2$\frac{\underline{\;高温\;}}{电炉}$Si+2CO b.3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
c.C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2 d.CO2+CH4$\stackrel{催化剂}{→}$CH3COOH
上述反应中,理论原子利用率最高的是d.可用碳酸钾溶液吸收b中生产的CO2,常温下,pH=10的碳酸钾溶液中水电离的OH-的物质的量浓度为1×10-4 mol•L-1,常温下,0.1mol•L-1KHCO3溶液的pH>8,则溶液中c(H2CO3)>c(CO32-)(填“>”,“=”或“<”).
(2)有机物加氢反应中镍是常用的催化剂.但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,查得资料如图1,
则:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-270kJ/mol.
(3)已知N2(g)+3H2(g)=2NH3(g)△H=-94.4kJ•mol-1,恒容时,体系中各物质浓度随时间变化的曲线如图2所示,各时间段最终均达平衡状态.
①在2L容器中发生反应,时段Ⅰ放出的热量为94.4kJ.
②25min时采取的措施是将NH3从反应体系中分离出去.
③时段Ⅲ条件下,反应的平衡常数为2.37(保留3位有效数字).
(4)电化学降解N的原理如图3所示.电源正极为A(填“A”或“B”),阴极反应式为2NO3-+12H++10e-=N2+6H2O.
分析 (1)反应物中的原子全部参加反应的,原子利用律最高,据此解答即可;水电离的OH-的物质的量浓度=$\frac{10{\;}^{-14}}{10{\;}^{-pH}}$;常温下,0.1mol•L-1 KHCO3溶液pH>8,说明碳酸氢根在水解程度大于电离程度;
(2)由图1可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
利用盖斯定律(i)-(ii)计算即可;
(3)①根据时段Ⅰ达到平衡时生成氨气的物质的量及热化学方程式N2(g)+3H2(g)?2NH3(g);△H=-94.4kJ•mol-1计算出放出的热量;
②根据25min时氨气的物质的量变为0,而氮气和氢气的物质的量不变进行解答,改变的条件是分离出氨气;
③根据时段Ⅲ条件下达到平衡时各组分的浓度及平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积进行解答;
(4)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极;在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有氢离子参与反应且有水生成.
解答 解:(1)观察四个反应方程式可见,只有反应d中参加反应的物质全部转化为一种物质,故原子利用率最高;
可用碳酸钾溶液吸收生成的CO2,常温下pH=10的碳酸钾溶液中水电离的c(OH-)=$\frac{10{\;}^{-14}}{10{\;}^{-pH}}$mol/L=1×10-4 mol•L-1;
常温下,0.1mol•L-1 KHCO3溶液pH>8,则溶液中碳酸氢根离子水解程度大于电离程度,所以c(H2CO3)>c(CO32-);
故答案为:d; 1×10-4 mol•L-1;>;
(2)由图1可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
(i)-(ii)得:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-563-(-298)=-270kJ•mol-1,故答案为:-270kJ/mol;
(3)①时段Ⅰ达到平衡时生成的氨气的物质的量为:1.00 mol/L×2L=2.00mol,
根据N2(g)+3H2(g)?2NH3(g);△H=-94.4kJ•mol-1可知生成2.00mol氨气放出的热量为94.4kJ,
故答案为:94.4kJ;
②25min时氨气的物质的量迅速变为0而氮气、氢气的物质的量不变,之后氮气、氢气的物质的量逐渐减小,氨气的物质的量逐渐增大,说明25min时改变的条件是将NH3从反应体系中分离出去,
故答案为:将NH3从反应体系中分离出去;
③时段Ⅲ条件下,反应为:N2(g)+3H2(g)?2NH3(g),图象方向可知平衡状态下[N2]=0.25mol/L,[NH3]=0.50mol/L,[H2]=0.75mol/L,该反应的化学平衡常数为:K=$\frac{[NH{\;}_{3}]{\;}^{2}}{[H{\;}_{2}]{\;}^{3}[N{\;}_{2}]}$=$\frac{(0.50mol/L){\;}^{2}}{(0.75mol/L){\;}^{3}×0.25mol/L}$=2.37,
故答案为:2.37;
(4)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极;在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有H2O参与反应且有水生成,
所以阴极上发生的电极反应式为:2NO3-+12H++10e-=N2+6H2O,
故答案为:A,2NO3-+12H++10e-=N2+6H2O.
点评 本题主要考查的是绿色化学的概念、盖斯定律的应用、影响化学平衡的因素及电解池工作原理,题目难度中等,明确化学平衡常数的概念及计算方法是解题关键.

| A. | 升高温度 | B. | 使用催化剂 | C. | 降低温度 | D. | 缩小容器体积 |
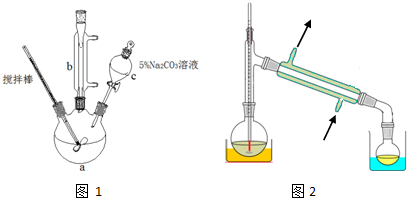
①取10.0g丙烯酸和6.0g甲醇放置于三颈烧瓶中,连接好冷凝管,用搅拌棒搅拌,水浴加热.
②充分反应后,冷却,向混合液中加入5%Na2CO3溶液洗至中性.
③分液,取上层油状液体,再用无水Na2SO4干燥后蒸馏,收集70-90℃馏分.
可能用到的信息:
| 沸点 | 溶解性 | ||
| 丙烯酸 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
| 甲醇 | 65℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
| 丙烯酸甲酯 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
(1)仪器c的名称是分液漏斗.
(2)混合液用5%Na2CO3溶液洗涤的目的是除去混合液中的丙烯酸和甲醇(降低丙烯酸甲酯的溶解度).
(3)请写出配制100g 5%Na2CO3溶液的所使用的玻璃仪器烧杯、玻璃棒、量筒.
(4)关于产品的蒸馏操作(夹持装置未画出),图2中有2处错误,请分别写出温度计水银球位置、尾接管与锥形瓶接口密封.
为检验产率,设计如下实验:
①将油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5mol/L的KOH溶液10.00mL,加热使之完全水解.
②用酚酞做指示剂,向冷却后的溶液中滴加0.5mol/L的HCl溶液,滴到终点时共消耗盐酸20.00mL.
(5)计算本次酯化反应丙烯酸的转化率54.0%.
(6)请列举2条本实验中需要采取的安全防护措施通风橱中实验、防止明火.
| A. | Na、Mg、Al元素最高化合价依次升高 | |
| B. | P、Cl最高价氧化物对应的水化物酸性增强 | |
| C. | N、O、F元素非金属性依次减弱 | |
| D. | Li、Na、K原子的电子层数依次增多 |

关于它的叙述正确的是( )
| A. | 维生素A的分子式为C20H32O | |
| B. | 维生素A可被催化氧化为醛 | |
| C. | 维生素A是一种易溶于水的醇 | |
| D. | 1mol维生素A在催化剂作用下最多可与7mol H2发生加成反应 |
