题目内容
3.将10mL某气态烃与过量40mLO2混合,点火使其充分反应,将反应后的气体混合物经干燥处理,剩余气体为30mL,在将气体通过足量的NaOH溶液,残留气体体积为10mL.试通过计算,得出该烃为何种物质.分析 将气体通过足量的NaOH溶液,残留气体体积为10mL,剩余为O2,说明消耗30mLO2,将反应后的气体混合物经干燥处理,剩余气体为30mL,可知生成CO2为20mL,以此解答该题.
解答 解:将气体通过足量的NaOH溶液,残留气体体积为10mL,剩余为O2,将反应后的气体混合物经干燥处理,剩余气体为30mL,可知生成CO2为20mL,同时说明消耗30mLO2,则有机物含有2个C原子,1mol烃消耗3molO2,
设烃的分子式为C2Hx,则2+$\frac{x}{4}$=3,x=4,
则应为C2H4,
答:该烃为乙烯.
点评 本题考查有机物的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握题给信息以及体积的变化,难度不大.

练习册系列答案
相关题目
13.实验室中的药品常按物质的性质、类别等有规律地摆放.现有部分药品按某种规律的摆放在实验桌上,如下图.做“硫酸的性质”的实验时,某同学取用BaCl2溶液后,应把它放回的位置是( )
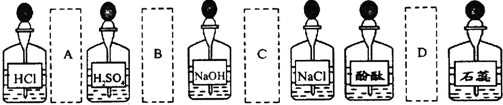

| A. | A | B. | B | C. | C | D. | D |
14.在从碘水中萃取碘的实验中,下列说法正确的是( )
| A. | 萃取剂要求不溶于水,且比水更容易使碘溶解 | |
| B. | 注入碘水和萃取剂,倒转分液漏斗反复用力振荡后立即分液 | |
| C. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| D. | 实验室如果没有四氯化碳,可以用酒精代替 |
11.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 16g O2和O3的混合气体中含有的原子数为NA | |
| B. | 在1L0.1 mol/L碳酸钠溶液中,CO32-总数为0.1 NA | |
| C. | 标准状况下,22.4 LSO3与水反应生成1mol硫酸 | |
| D. | 标准状况下,22.4L Cl2完全发生氧化还原反应一定转移2NA个电子 |
8.下列叙述中正确的是( )
| A. | 氯原子、氯离子、氯气均为黄绿色,且氯离子比氯原子结构稳定 | |
| B. | 氯原子易得电子,所以Cl2在化学反应中氯元素化合价只会降低 | |
| C. | 氯原子、氯离子、氯气分子中原子的最外层均达到8电子结构 | |
| D. | 氯元素在自然界中不存在游离态,只以化合态形式存在 |
 ,该化合物中化学键类型有离子键、共价键.
,该化合物中化学键类型有离子键、共价键. .
.