题目内容
12.下列说法正确的是( )| A. | 燃料的燃烧都是放热反应 | |
| B. | 氯化钾的电子式为: | |
| C. | 决定化学反应速率的主要因素是反应物的浓度 | |
| D. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 |
分析 A.燃烧反应放出大量的能量;
B.氯化钾为离子化合物;
C.决定化学反应速率的主要因素是物质的本身的性质;
D.氯化氢为共价化合物.
解答 解:A.燃烧反应放出大量的能量,为放热反应,故A正确;
B.氯化钾为离子化合物,电子式为 ,故B错误;
,故B错误;
C.决定化学反应速率的主要因素是物质的本身的性质,浓度等为次要因素,故C错误;
D.氯化氢为共价化合物,在水分子的作用下电离,属于电解质,故D错误.
故选A.
点评 本题考查较为综合,涉及化学反应与能量 变化、电子式、化学反应速率以及化学键等知识,为高考常见题型,侧重考查学生的分析能力,注意把握相关基础知识的学习与积累,难度不大.

练习册系列答案
相关题目
1.有关工业合成氨的说法正确的是( )
| A. | 使用催化剂的目的是提高反应物的转化率 | |
| B. | 循环使用N2、H2的目的是提高氨的产率 | |
| C. | 温度控制在500℃左右的目的是有利于化学平衡向正反应方向移动 | |
| D. | 高压下反应有利于增大反应速率,所以压强越高越好 |
3.下列有关能量变化的说法中不正确的是( )
| A. | 化学反应必伴随能量变化 | |
| B. | 反应是放热还是吸热取决于反应物和生成物具有的总能量的相对大小 | |
| C. | 可燃物燃烧和酸碱中和反应都是典型的放热反应 | |
| D. | 燃煤发电不需经过其它能量转换过程,可直接把化学能转化为电能 |
20.试分析有机物下列性质中该有机物不具有的是:( )

(1)加聚反应(2)加成反应 (3)使酸性高锰酸钾溶液褪色
(4)与NaHCO3溶液反应放出CO2气体 (5)与KOH溶液反应.

(1)加聚反应(2)加成反应 (3)使酸性高锰酸钾溶液褪色
(4)与NaHCO3溶液反应放出CO2气体 (5)与KOH溶液反应.
| A. | (1)(3) | B. | (2)(4) | C. | (4) | D. | (4)(5) |
7.下列有关有机物的叙述正确的是( )
| A. | 毛织、丝织衣服不宜用加酶洗衣粉洗涤 | |
| B. | 纤维素、淀粉、油脂均为天然高分子化合物 | |
| C. | 由煤的干馏可知煤中含甲苯、二甲苯、苯酚等芳香族化合物 | |
| D. | 向蛋白质溶液中滴入CuSO4溶液,蛋白质聚沉后还能溶于水 |
4.一定温度下,将一定量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )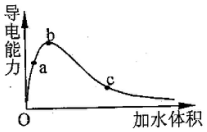

| A. | a,b,c三点溶液的pH:a>b>c | |
| B. | 若用湿润的pH试纸测试c处溶液的pH,比实际的pH偏小 | |
| C. | a,b,c三点溶液用1mol•L-1的NaOH溶液中和,消耗NaOH溶液的体积a>b>c | |
| D. | a,b,c点醋酸的电离程度:c>b>a |
13.关于下列有机物,说法正确的是( )
| A. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| B. | 按系统命名法, 的名称为4,4-二甲基-3-乙基己烷 的名称为4,4-二甲基-3-乙基己烷 | |
| C. | 满足分子式为C4H8ClBr的有机物有11种 | |
| D. | 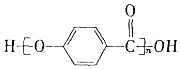 的结构中含有酯基 的结构中含有酯基 |
14.用NA代表阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,1.12 L戊烷所含共价键数目为0.8NA | |
| B. | 1 L 0.1 mol/L (NH4)2SO4溶液中含N原子数为0.2NA | |
| C. | 2.2 gD218O与T2O的混合物中所含质子数、中子数均为NA | |
| D. | 一定量的浓硫酸与足量锌共热,产生22.4L气体时,转移的电子数一定为2NA |