题目内容
2.亚氯酸钠(NaClO2)是重要的含氯消毒剂,工业上主要有吸收法和电解法两种制取方法.生产过程中生成的ClO2气体不稳定,浓度高时易爆炸.简易工艺流程如下所示:下列说法中不正确的是( )
| A. | 空气的只要作用是提供氧气作氧化剂 | |
| B. | 电解法中ClO2在阴极发生的电极反应式为:ClO2+Na++e-=NaClO2 | |
| C. | 吸收法中加入H2O2主要是做还原剂 | |
| D. | 从环保的角度考虑,电解法比吸收法更环保 |
分析 A.ClO2气体很不稳定,浓度高时易爆炸,发生器中鼓入空气,可起到稀释浓度的作用;
B.ClO2生成ClO2-,应被还原;
C.ClO2还原为ClO2-,所以过氧化氢是还原剂;
D.电解法中氯离子在阳极失电子生成氯气.
解答 解:A.由信息可知,纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全.发生器中鼓入空气的作用应是稀释ClO2以防止爆炸,所以作用不只是提供氧气作氧化剂,故A错误;
B.ClO2生成ClO2-,应被还原,在阴极生成,电极方程式为ClO2+e-=ClO2-,故B错误;
C.过氧化氢可用作还原剂将ClO2还原为ClO2-,故C正确;
D.电解法中氯离子在阳极失电子生成有毒的氯气,所以从环保的角度考虑,吸收法比电解法更环保,故D错误;
故选C.
点评 本题以学生比较陌生的亚氯酸钠制备为背景,以过氧化氢法制备亚氯酸钠为主线,考查学生阅读题目获取信息的能力、对浓度概念的理解、对氧化还原反应相关知识的运用、有关实验操作和简单实验设计能力考查以及在新情境下综合运用知识解决问题的能力,题目有一定的难度.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
12.雷雨天闪电时空气中有臭氧(O3)生成,下列说法中不正确的是( )
| A. | O2和O3互为同素异形体 | B. | O3是由3个氧原子构成的化合物 | ||
| C. | O2和O3相互转化属于化学变化 | D. | O3的摩尔质量为48g.mol-1 |
13.海水是个巨大的宝库,下列关于海水综合利用的说法不正确的是( )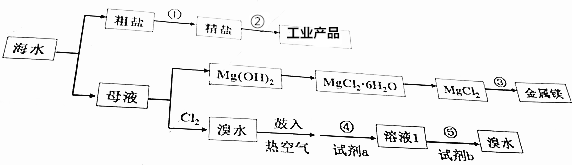

| A. | 步骤①中,除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaO溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸 | |
| B. | 步骤②的工业产品包括:H2、Cl2、NaOH、Na | |
| C. | 步骤③的方法为点解饱和MgCl2溶液 | |
| D. | 步骤④、⑤中,若试剂a为SO2水溶液,则试剂b可以是Cl2 |
17.W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18.下列说法正确的是( )
| A. | W、X只能形成一种化合物 | B. | 氧化物的水化物的酸性:Y<Z | ||
| C. | 离子半径:Y>Z>X | D. | X与Y不能存在于同一离子化合物中 |
7.短周期元素X、Y、Z、W、R的原子序数依次增大,X单质在暗处与H2剧烈化合并发生爆炸,Y位于第IA族,Z所处的周期序数与族序数相等,W元素最高正价与最低负价和为0,R与X同族,则下列说法正确的是( )
| A. | 原子半径:Z>Y>X | |
| B. | X与R的核电荷数相差8 | |
| C. | 最高价氧化物对应的水化物的酸性:X>R | |
| D. | Y与Z两者最高价氧化物对应的水化物互不反应 |
 铁氰化钾{K3[Fe(CN)6]}俗称赤血盐,常用于检验Fe3+,遇Fe2+生成深蓝色沉淀,离子反应方程式为:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓.回答下列问题:
铁氰化钾{K3[Fe(CN)6]}俗称赤血盐,常用于检验Fe3+,遇Fe2+生成深蓝色沉淀,离子反应方程式为:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓.回答下列问题:
 ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是_________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是_________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。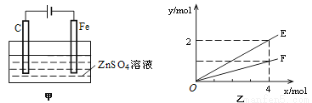
 2H2(g)+O2(g)ΔH1=571.6kJ/mol
2H2(g)+O2(g)ΔH1=571.6kJ/mol