题目内容
9.已知氯化钠和纯碱晶体的溶解度曲线如下:将碱从氯化钠和纯碱的混合物中分离出来,最好应用的方法是( )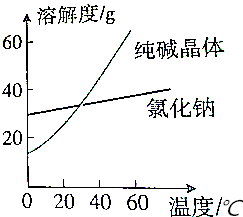
| A. | 蒸馏法 | B. | 苹取法 | C. | 结晶法 | D. | 分液法 |
分析 两种溶质的溶解度随温度 变化不同,可用结晶法分离,以此解答该题.
解答 解:由图可知,氯化钠溶解度受温度影响较小,碳酸钠溶解度受温度影响大,利用冷却热饱和溶液分离,即用热水把固体溶解配制成饱和溶液,等液体冷却后,因为碳酸钠的溶解度随温度变化大,而NaCl小,所以碳酸钠析出,而氯化钠留在母液当中,为结晶法.
而蒸馏用于分离沸点不同的物质,萃取分离溶质在有机溶剂的较大的物质,分液用于分离互不相溶的物质,都不适合碳酸钠与氯化钠的分离.
故选C.
点评 本题考查物质的分离,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质的异同以及常见物质的分离操作原理、方法,难度不大.

练习册系列答案
相关题目
19.有下列物质:①甲烷;②苯;③聚乙烯;④乙烯;⑤乙炔;⑥甲苯既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ④⑤ | B. | ②④⑤ | C. | ④⑤⑥ | D. | ③④⑤ |
20.一定温度下,下列溶液的离子浓度关系式正确的是( )
| A. | pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol•L-1 | |
| B. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a>b+1 | |
| C. | pH=9的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):①>③>② | |
| D. | pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-) |
4.适当可以加热,只用一种试剂就可以鉴别的物质组是( )
| A. | NaCl、KNO3、AlCl3、Fe(NO3)3 | B. | Fe、FeO、CuO、FeS、CuS、MnO2 | ||
| C. | MgCl2、FeCl2、KCl、AlCl3、NH4Cl | D. | K2CO3、NaI、Na2CO3、NaCl、Na2SO4 |
4.下列离子方程式正确的是( )
| A. | 碘化钾溶液中加入浓溴水2I-+Br2═2Br-+I2 | |
| B. | 小苏打与盐酸反应CO32-+2H+═CO2↑+H2O | |
| C. | 氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
11.NA为阿伏伽德罗常数,下列说法中正确的是( )
| A. | 高温下60gSiO2与足量纯碱反应,最多释放出2NA个气体分子 | |
| B. | 1molC5H12分子中共价键总数为14NA | |
| C. | 78gNa2O2固体与足量的H2O反应转移的电子数为NA | |
| D. | 标准状况下,2.24LNH3和CH4的混合气体,所含电子总数为2NA |
8.下列实验方法能达到目的是( )
| A. | 用焰色反应鉴別Na2CO3溶液和K2CO3溶液 | |
| B. | 用分液漏斗分离食醋中的乙酸与水 | |
| C. | 用丁达尔现象检验NaCl溶液中是否含有淀粉胶体 | |
| D. | 用NaOH溶液除去Cl2中混有的少量HCl |
9.下列物质中既能跟酸反应,又能跟碱溶液反应的是( )
①NaHCO3 ②SiO2 ③Al(OH)3 ④Al.
①NaHCO3 ②SiO2 ③Al(OH)3 ④Al.
| A. | 全部 | B. | ①③④ | C. | ②③④ | D. | ③④ |