题目内容
2.下列是实验室以硫酸铝为原料来制取一定量Al2O3某些操作,其中能达到实验目的是( )| A. | 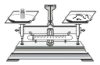 称取样品 | B. |  溶解样品 | ||
| C. | 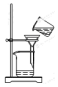 分离Al(OH)3沉淀 | D. |  灼烧氢氧化铝沉淀 |
分析 A.称量时,遵循左物右码;
B.在烧杯中溶解固体且不断搅拌;
C.过滤需要玻璃棒引流;
D.灼烧应在坩埚中进行.
解答 解:A.称量时,遵循左物右码,图中位置颠倒,故A错误;
B.在烧杯中溶解固体且不断搅拌,图中操作合理,故B正确;
C.过滤需要玻璃棒引流,图中缺少玻璃棒,故C错误;
D.灼烧氢氧化铝在坩埚中进行,不能使用蒸发皿,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握固体的称量、实验基本操作、混合物分离、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
12.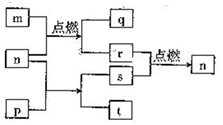 短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )
短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )
 短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )
短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )| A. | Y、Z、W的简单离子半径:W>Z>Y | B. | 最高价氧化物的水化物的碱性:Z>W | ||
| C. | 简单气态氢化物的热稳定性:X>Y | D. | Y与Z形成的化合物中不含有共价键 |
13.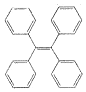 TPE及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛.TPE的结构简式如图,下列关于TPE的说法正确的是( )
TPE及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛.TPE的结构简式如图,下列关于TPE的说法正确的是( )
 TPE及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛.TPE的结构简式如图,下列关于TPE的说法正确的是( )
TPE及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛.TPE的结构简式如图,下列关于TPE的说法正确的是( )| A. | TPE属于苯的同系物 | |
| B. | TPE能发生加成反应,但不能取代反应 | |
| C. | TPE与化合物 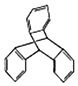 互为同分异构体 互为同分异构体 | |
| D. | TPE的一氯代物有3种 |
10.原子序数依次增大的短周期元素A、B、C、D,其中A、C同主族,B、D同周期,A原子的最外层电子数是其电子层数的3倍,B原子核外各层电子数之比为1:4:2,D原子很活泼.下列判断正确的是( )
| A. | 形成简单离子的离子半径为D>C>A | |
| B. | 四种元素形成的简单氢化物中,D的沸点最高 | |
| C. | B的氧化物对应水化物为弱酸,C和D的氧化物对应水化物均为强酸 | |
| D. | C和D形成的某种化合物具有8电子稳定结构,其化学式可能是C2D2 |
17.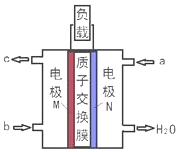 甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式2CH4O+3O2═2CO2+4H2O,下图是该燃料电池的示意图.下列说法正确的是( )
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式2CH4O+3O2═2CO2+4H2O,下图是该燃料电池的示意图.下列说法正确的是( )
 甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式2CH4O+3O2═2CO2+4H2O,下图是该燃料电池的示意图.下列说法正确的是( )
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式2CH4O+3O2═2CO2+4H2O,下图是该燃料电池的示意图.下列说法正确的是( )| A. | a是甲醇燃料、b是氧气 | |
| B. | 当转移6mol e-时,消耗33.6L O2 | |
| C. | 负极反应:CH4O-6e-+H2O═CO2↑+6H+ | |
| D. | 质子从N电极区穿过交换膜移向M电极区 |
7.有一未知浓度的硫酸溶液50mL,在加入0.5mol/L Ba(NO3)2溶液25mL后,改加NaOH溶液,结果用去1.0mol/L NaOH溶液50mL恰好完全中和,则硫酸的物质的量浓度是( )
| A. | 0.5 mol/L | B. | 1.0 mol/L | C. | 1.5 mol/L | D. | 2.0 mol/L |
4.用作麻醉剂的氯仿(CHCl3)常因保存不慎而被空气氧化,产生剧毒的光气(COCl2),反应的化学方程式为2CHCl3+O2═2HCl+2COCl2.为了防止事故,使用前可用于检验氯仿是否变质的试剂是(注:CHCl3不与AgNO3溶液反应产生沉淀)( )
| A. | 酚酞试液 | B. | 用石蕊溶液 | ||
| C. | NaOH溶液 | D. | 用硝酸酸化后的AgNO3溶液 |
5.常温下,下列说法正确的是( )
| A. | 0.1mol•L-1的氯化铵溶液中:c(NH4+)>c(Cl-)>c(H+)>c(OH-) | |
| B. | 0.1mol•L-1的硫化钠溶液中:c(Na+)=2c(S2-)+c(HS-)+c(H2S) | |
| C. | 在NaHCO3溶液中加入与其等物质的量的NaOH后:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 物质的量浓度相等的CH3COOH和NaOH溶液等体积混合后:c(CH3COOH)+c(H+)=c(OH-) |