题目内容
7.有一未知浓度的硫酸溶液50mL,在加入0.5mol/L Ba(NO3)2溶液25mL后,改加NaOH溶液,结果用去1.0mol/L NaOH溶液50mL恰好完全中和,则硫酸的物质的量浓度是( )| A. | 0.5 mol/L | B. | 1.0 mol/L | C. | 1.5 mol/L | D. | 2.0 mol/L |
分析 硝酸钡不影响氢离子的物质的量,反应实质为H2SO4 +2NaOH=Na2SO4+2H2O,根据氢氧化钠的物质的量计算出硫酸的物质的量,然后根据c=$\frac{n}{V}$计算出硫酸的物质的量浓度.
解答 解:Ba(NO3)2溶液不与硫酸中氢离子反应,发生反应实质为:H2SO4 +2NaOH=Na2SO4+2H2O,则n(H2SO4)=$\frac{1}{2}$n(NaOH)=$\frac{1}{2}$×1.0mol/L×0.05L=0.025mol,
所以该硫酸的物质的量浓度为:c(H2SO4)=$\frac{0.025mol}{0.05L}$=0.5mol/L,
故选A.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确发生反应实质为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
2.下列是实验室以硫酸铝为原料来制取一定量Al2O3某些操作,其中能达到实验目的是( )
| A. | 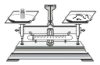 称取样品 | B. |  溶解样品 | ||
| C. | 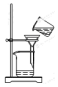 分离Al(OH)3沉淀 | D. |  灼烧氢氧化铝沉淀 |
2.下列关于中和热测定的实验描述正确的是( )
| A. | 需要用到的仪器是酒精灯,烧杯,温度计,量筒,环形玻璃搅拌棒 | |
| B. | 中和热测定可以是所有的酸和碱 | |
| C. | 环形玻璃搅拌棒的搅拌方式是上下搅动 | |
| D. | 实验所取NaOH物质的量稍大于HCl,会导致中和热的数值偏高 |
19.在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混合气体,活塞恰好停留在离左端的$\frac{1}{4}$处(如图左所示),然后引燃氢、氧混合气体,反应完毕后恢复至原来温度,活塞恰好停在中间(如图所示),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是( )
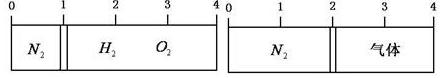

| A. | 3:4 | B. | 4:5 | C. | 6:2 | D. | 2:7 |
16.有pH均为2的a盐酸、b醋酸两瓶溶液,与足量锌反应放出等体积H2所需时间的长短顺序是a>b(用“>”、“<”、“=”表示,下同);完全中和等物质的量的NaOH溶液需两种酸的体积大小顺序是a>b.
17.生活中处处有化学,请你根据所学知识,判断下列说法错误的是( )
| A. | 为防止流感传染,可将教室门窗关闭后,用食醋熏蒸,进行消毒 | |
| B. | 医疗上常用高温煮蒸的方法对医疗器械进行消毒 | |
| C. | 生活中常用在豆浆中加入少量石膏的方法来使豆浆凝固制作豆腐 | |
| D. | 对环境进行消毒的原理是使细菌变性,可以用浓HNO3代替“84”消毒液 |
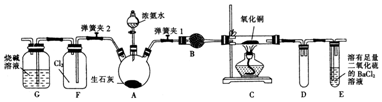
 硫及其化合物是重要的化工原料,在工农业生产应用广泛.
硫及其化合物是重要的化工原料,在工农业生产应用广泛. 在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4固体混合物,加热充分反应.加入的混合物质量和产生的气体体积(标准状况)的关系如图.
在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4固体混合物,加热充分反应.加入的混合物质量和产生的气体体积(标准状况)的关系如图.