题目内容
某同学称取9.00g淀粉溶于水,测定淀粉的水解百分率.其程序如下:

试回答下列问题:
(1)各步加入的试剂为:A ,B ,C .
(2)加入A溶液而不加入B溶液是否可以 ,其理由是 .
(3)写出淀粉水解的方程式 .
(4)当析出1.44g砖红色沉淀时,淀粉水解率是 .[已知葡萄糖与Cu(OH)2反应的化学方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O↓+2H2O].

试回答下列问题:
(1)各步加入的试剂为:A
(2)加入A溶液而不加入B溶液是否可以
(3)写出淀粉水解的方程式
(4)当析出1.44g砖红色沉淀时,淀粉水解率是
| △ |
考点:蔗糖与淀粉的性质实验
专题:
分析:(1)淀粉在酸性条件下水解生成葡萄糖,加碱中和之后溶液呈碱性,然后加入新制的氢氧化铜,有砖红色沉淀可检验产物葡萄糖;淀粉遇碘单质变蓝;
(2)葡萄糖与新制氢氧化铜反应应该在碱性环境下进行;
(3)淀粉为多糖,水解生成葡萄糖;
(4)依据1mol-CHO~1molCu2O,根据生成的Cu2O质量求出水解的淀粉的质量,淀粉的水解率=
×100%.
(2)葡萄糖与新制氢氧化铜反应应该在碱性环境下进行;
(3)淀粉为多糖,水解生成葡萄糖;
(4)依据1mol-CHO~1molCu2O,根据生成的Cu2O质量求出水解的淀粉的质量,淀粉的水解率=
| 以水解的淀粉的质量 |
| 淀粉的总质量 |
解答:
解:(1)淀粉在稀硫酸作用下水解生成葡萄糖,加Na0H溶液中和稀硫酸,使混合液呈碱性,制备氢氧化铜沉淀,加入新制氢氧化铜溶液,加热至沸腾生成红色沉淀,证明淀粉已水解,由水解后的溶液加碘水变蓝,则说明水解不完全;
故答案为:H2SO4;NaOH;Cu(OH)2县浊液;
(2)葡萄糖与新制氢氧化铜反应应该在碱性环境下进行,加Na0H溶液的作用是中和稀硫酸,使混合液呈碱性,
故答案为:不可以;葡萄糖与氢氧化铜的反应必须在碱性条件下才能进行;
(3)淀粉在酸性环境下水解的最终产物是葡萄糖,淀粉水解的方程式为:(C6H10O5)n+n H2O
n C6H12O6;
故答案为:(C6H10O5)n+n H2O
n C6H12O6;
(4)淀粉水解的方程式为:(C6H10O5)n(淀粉)+nH2O
nC6H12O6(葡萄糖),
一元醛与新制氢氧化铜反应的方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+2H2O+Cu2O↓,
设水解的淀粉的质量为x则:
(C6H10O5)n~nC6H12O6~nCu2O
162n 144n
x 1.44 g
x=
=1.62g;
淀粉的水解率=
×100%=
×100%=18%;
故答案为:18%.
故答案为:H2SO4;NaOH;Cu(OH)2县浊液;
(2)葡萄糖与新制氢氧化铜反应应该在碱性环境下进行,加Na0H溶液的作用是中和稀硫酸,使混合液呈碱性,
故答案为:不可以;葡萄糖与氢氧化铜的反应必须在碱性条件下才能进行;
(3)淀粉在酸性环境下水解的最终产物是葡萄糖,淀粉水解的方程式为:(C6H10O5)n+n H2O
| 稀硫酸 |
故答案为:(C6H10O5)n+n H2O
| 稀硫酸 |
(4)淀粉水解的方程式为:(C6H10O5)n(淀粉)+nH2O
| 稀硫酸 |
一元醛与新制氢氧化铜反应的方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2
| △ |
设水解的淀粉的质量为x则:
(C6H10O5)n~nC6H12O6~nCu2O
162n 144n
x 1.44 g
x=
| 162n×1.44g |
| 144n |
淀粉的水解率=
| 以水解的淀粉的质量 |
| 淀粉的总质量 |
| 1.62g |
| 9g |
故答案为:18%.
点评:本题考查了淀粉、葡萄糖的性质以及相关计算,题目难度不大,解题时注意淀粉水解的条件和醛与新制氢氧化铜反应的条件.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
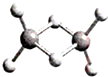 近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法错误的是( )
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法错误的是( )| A、氢铝化合物与水反应生成氢氧化铝和氢气 |
| B、Al2H6中含有离子键和极性共价键 |
| C、氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| D、氢铝化合物中可能存在组成为AlnH2n+2的物质(n为正整数) |
向含有1mol明矾的溶液中逐滴加入Ba(OH)2溶液,充分反应,下列说法不正确的是( )
| A、当Al3+恰好完全沉淀时,消耗Ba(OH)2 1.5mol |
| B、当SO42-恰好完全沉淀时,Al3+全部转化为AlO2- |
| C、随着加入的Ba(OH)2的物质的量不断增大,沉淀的物质的量不断增大 |
| D、当向溶液中加入1.5mol Ba(OH)2时,反应可用离子方程式2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓表示 |
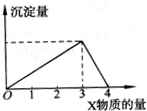 将X气体(或溶液)慢慢通入(或加入)一定量的Y溶液中,产生沉淀量与加入X的物质的量(mol)的关系如图所示,符合如图情况的是( )
将X气体(或溶液)慢慢通入(或加入)一定量的Y溶液中,产生沉淀量与加入X的物质的量(mol)的关系如图所示,符合如图情况的是( )| A、X为NaOH溶液,Y为Al2(SO4)3溶液 |
| B、X为CO2,Y为Ca(OH)2溶液 |
| C、X为NH3,Y为AlCl3溶液 |
| D、X为HCl溶液,Y为Na[Al(OH)4]溶液 |
下列物质中能水解,且最终产物为两种有机物的是( )
| A、葡萄糖 | B、淀粉 |
| C、蔗糖 | D、纤维素 |
对于在一定条件下进行的化学反应:2SO2+O2?2SO3,改变下列条件,可以提高反应物中活化分子百分数的是( )
| A、增大压强 |
| B、降低温度 |
| C、加入催化剂 |
| D、减小反应物浓度 |
