��Ŀ����
һ���¶��£����Ϊ2L���ܱ�������X��Y��Z��������ij�ʼ���ʵ�����ƽ�����ʵ������������˵����ȷ���ǣ�������
| ���� | X | Y | Z |
| ��ʼ���ʵ�����mol�� | 0.2 | 0.2 | 0 |
| ƽ�����ʵ�����mol�� | 0.1 | 0.05 | 0.1 |
| A����Ӧ�ɱ�ʾΪ2X+3Y?2Z����ƽ�ⳣ��Ϊ8000 |
| B������ѹǿʹƽ��������Z�ķ����ƶ���ƽ�ⳣ������ |
| C���������������ѹ����1L����X�����������С��Ũ������ |
| D���������¶�ʱ��Z��Ũ������֪�¶�����ʱ����Ӧ���������淴Ӧ���ʼ�С��ƽ�⳯����Ӧ�����ƶ� |
���㣺��ѧƽ��ļ���
ר�⣺
������A��Ũ�ȱ仯��֮�ȵ��ڻ�ѧ������֮�ȣ��ݴ��жϻ�ѧ����ʽ��
B������ѹǿʹƽ�������������С�ķ����ƶ���ƽ�ⳣ��ֻ���¶��йأ�
C���������������ѹ����1L��ѹǿ����ƽ�����ƣ�
D�������¶ȣ����淴Ӧ���ʾ�����
B������ѹǿʹƽ�������������С�ķ����ƶ���ƽ�ⳣ��ֻ���¶��йأ�
C���������������ѹ����1L��ѹǿ����ƽ�����ƣ�
D�������¶ȣ����淴Ӧ���ʾ�����
���
�⣺A����ѧ������֮�ȵ���Ũ�ȱ仯��֮�ȣ�����c��X������c��Y������c��Z����=0.1��0.15��0.1=2��3��2����Ӧ�ķ���ʽΪ2X+3Y?2Z��
ƽ�ⳣ��k=
=
=1600����A����
B����Ӧ�ķ���ʽΪ2X+3Y?2Z������ѹǿʹƽ��������Z�ķ����ƶ���ƽ�ⳣ��ֻ���¶��йأ��¶Ȳ��䣬ƽ�ⳣ�����䣬��B����
C���������������ѹ����1L��ѹǿ����ƽ�����ƣ�X�����������С��������������ԭ����XŨ���������ջ������ӣ���C��ȷ��
D�������¶ȣ�Z��Ũ������ƽ�⳯����Ӧ�����ƶ���������Ӧ��������D����
��ѡ��C��
ƽ�ⳣ��k=
| c2(z) |
| c2(x)?c2(y) |
(
| ||||
(
|
B����Ӧ�ķ���ʽΪ2X+3Y?2Z������ѹǿʹƽ��������Z�ķ����ƶ���ƽ�ⳣ��ֻ���¶��йأ��¶Ȳ��䣬ƽ�ⳣ�����䣬��B����
C���������������ѹ����1L��ѹǿ����ƽ�����ƣ�X�����������С��������������ԭ����XŨ���������ջ������ӣ���C��ȷ��
D�������¶ȣ�Z��Ũ������ƽ�⳯����Ӧ�����ƶ���������Ӧ��������D����
��ѡ��C��
���������⿼�黯ѧƽ����йؼ��㡢��Ӧ���ʼ��㡢ƽ���ƶ�Ӱ�����صȣ��ѶȽϴ�ȷ������ʽ�ǽ���ؼ���

��ϰ��ϵ�д�
�����Ŀ
��4mol A �����2mol B��������1L���ܱ������У���Ϻ������·�Ӧ��2A��g��+B��g���T2C��g��������2s����C��Ũ��Ϊ1.2mol/L������˵����ȷ���ǣ�������
| A��������A��ʾ�ķ�Ӧ����Ϊ1.2 mol/��L?s�� |
| B��2 sʱ����A��ת����Ϊ30% |
| C��������B��ʾ�ķ�Ӧ����Ϊ0.6 mol/��L?s�� |
| D��2 sʱ����B��Ũ��Ϊ0.6 mol/L |
���и��������ܴ�����������Һ��ɫΪ��ɫ���ǣ�������
| A��Na+��MnO4-��K+��NO3-��SO32- |
| B��Na+��CO32-��Cl-��Al3+��NO3- |
| C��Na+��S2-��OH-��K+��Cl-��NO3- |
| D��Fe2+��H+��Na+��Ca2+��NO3- |
����ͬ���¶��£�100mL 0.01mol?L-1������Һ��10mL 0.1mol?L-1������Һ��Ƚϣ�������ֵ��ǰ�ߴ��ں��ߵ��ǣ�������
| A���к�ʱ�����������Ƶ����ʵ��� |
| B��H+�����ʵ���Ũ�� |
| C������ƽ�ⳣ��K |
| D��H+�����ʵ��� |
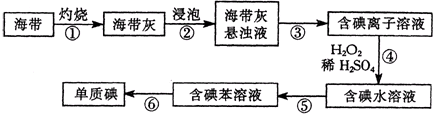
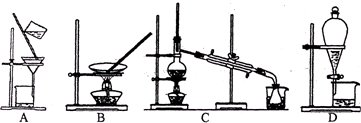
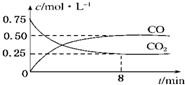 ij�¶��£���һ�ܱ������г���һ����CO2���������������ۣ�������Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g�������CO2��COŨ����ʱ��ı仯��ͼ��ʾ��
ij�¶��£���һ�ܱ������г���һ����CO2���������������ۣ�������Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g�������CO2��COŨ����ʱ��ı仯��ͼ��ʾ��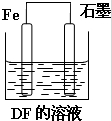 A��B��C��D��E��F���ֶ���������Ԫ�أ���ԭ��������������A��Dͬ���壻A��B��C�����γɶ��ֳ�����10����������ͬһ�����У������Ӱ뾶E����С��ԭ�Ӱ뾶F����С��B�ĵ��ʷ����������Թ��õ��Ӷԣ���ش��������⣺
A��B��C��D��E��F���ֶ���������Ԫ�أ���ԭ��������������A��Dͬ���壻A��B��C�����γɶ��ֳ�����10����������ͬһ�����У������Ӱ뾶E����С��ԭ�Ӱ뾶F����С��B�ĵ��ʷ����������Թ��õ��Ӷԣ���ش��������⣺