题目内容
8.X、Y、Z、M为4种短周期元素,X、Y位于同周期且原子半径r(X)>r(Y),Y2-与M+的电子层结构相同,Z与X的原子核外最外层电子数相同,Z的单质可制成半导体材料.下列说法不正确的是( )| A. | 由元素X与Z形成的化合物中只含共价键 | |
| B. | XY2、ZY2、M2Y2的晶体分别属于3种不同类型的晶体 | |
| C. | 单质M的晶体是体心立方堆积,M的配位数是8 | |
| D. | X的氢化物X2H2分子中含有2个σ键和3个π键 |
分析 X、Y、Z、M为4种短周期元素,Z的单质可制成半导体材料,可知Z为Si元素;Y2-与M+的电子层结构相同,可知M为Na,Y为O,Z与X的原子核外最外层电子数相同,X、Y位于同周期且原子半径r(X)>r(Y),则X为C,以此来解答.
解答 解:由上述分析可知,X为C,Y为O,Z为Si,M为Na,
A.由元素X与Z形成的化合物为SiC,只含共价键,故A正确;
B.CO2、SiO2、Na2O2的晶体分别为分子晶体、原子晶体、离子晶体,属于3种不同类型的晶体,故B正确;
C.单质Na的晶体和K相似,是体心立方堆积,Na的配位数是8,故C正确;
D.C的氢化物C2H2分子中的结构式为H-C≡C-H,含有3个σ键和2个π键,故D错误;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子序数、原子结构推断元素为解答的关键,侧重分析与推断能力的考查,注意晶体类型及化学键的判断,题目难度不大.

练习册系列答案
相关题目
18.把17.1g Ba(OH)2固体分别加入到100mL 1mol/L的下列物质的溶液中,溶液导电能力变化最小的是( )
| A. | 醋酸 | B. | 碳酸钠溶液 | C. | CuSO4溶液 | D. | KCl溶液 |
19.据《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)═SiO2(s)△H=-989.2kJ•mol-1,有关键能数据如表:
已知1mol Si中含2mol Si-Si键,1mol SiO2中含4mol Si-O键,则x的值为460.
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等.硅光电池是一种把光能转化为电能的装置.
(3)假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥当的是D(填字母).
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.硅的来源丰富,易于开采,且可再生
C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
D.寻找高效新催化剂,使硅的生产耗能很低,是硅能源开发利用的关键技术
(4)工业制备纯硅的反应为2H2(g)+SiCl4(g)═Si(s)+4HCl(g)△H=+240.4kJ•mol-1,生成的HCl通入100mL 1mol•L-1的NaOH溶液恰好反应,则反应过程中吸收(填“吸收”或“释放”)的热量为6.01kJ.
| 化学键 | Si-O | O═O | Si-Si |
| 键能/kJ•mol-1 | x | 498.8 | 176 |
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等.硅光电池是一种把光能转化为电能的装置.
(3)假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥当的是D(填字母).
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.硅的来源丰富,易于开采,且可再生
C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
D.寻找高效新催化剂,使硅的生产耗能很低,是硅能源开发利用的关键技术
(4)工业制备纯硅的反应为2H2(g)+SiCl4(g)═Si(s)+4HCl(g)△H=+240.4kJ•mol-1,生成的HCl通入100mL 1mol•L-1的NaOH溶液恰好反应,则反应过程中吸收(填“吸收”或“释放”)的热量为6.01kJ.
16.化学在生产和日常生活中有着重要的作用,下列有关说法不正确的是( )
| A. | 硅酸钠的水溶液俗称水玻璃,可用作木材防火剂 | |
| B. | “地沟油”经过加工处理后,可以用来制肥皂 | |
| C. | 含磷污水是很好的肥料,可灌溉庄稼,可直接排放到自然界水体中 | |
| D. | Fe2O3常用于生产红色油漆和涂料 |
13.两气体A和B的摩尔质量之比为2:1,则它们在同温、同压、同体积时的分子个数比应为( )
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 4:1 |
20.下列溶液中能大量共存的微粒的是( )
| A. | 无色溶液中可能大量存在:Al3+、NH4+、S2-、Cl- | |
| B. | 酸性溶液中可能大量存在:I-、ClO-、SO42-、Na+ | |
| C. | 中性溶液中可能大量存在:SO42-、K+、Fe3+、Cl- | |
| D. | 弱碱性溶液中可能大量存在:Na+、K+、Cl-、HCO3- |
18.盐是一类常见的物质,下列物质可直接反应生成盐的是( )
①金属 ②非金属 ③酸 ④碱 ⑤酸性氧化物 ⑥碱性氧化物.
①金属 ②非金属 ③酸 ④碱 ⑤酸性氧化物 ⑥碱性氧化物.
| A. | 只有③④ | B. | 只有①② | C. | 只有①③⑤ | D. | 全部 |
 硼、碳、氮、氟、硫、铁等元素的化合物广泛存在于自然界,回答下列问题:
硼、碳、氮、氟、硫、铁等元素的化合物广泛存在于自然界,回答下列问题: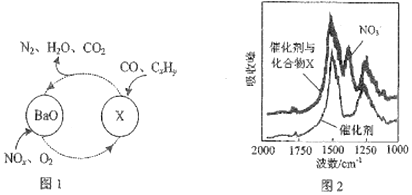
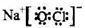 .
.