题目内容
19.据《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)═SiO2(s)△H=-989.2kJ•mol-1,有关键能数据如表:| 化学键 | Si-O | O═O | Si-Si |
| 键能/kJ•mol-1 | x | 498.8 | 176 |
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等.硅光电池是一种把光能转化为电能的装置.
(3)假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥当的是D(填字母).
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.硅的来源丰富,易于开采,且可再生
C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
D.寻找高效新催化剂,使硅的生产耗能很低,是硅能源开发利用的关键技术
(4)工业制备纯硅的反应为2H2(g)+SiCl4(g)═Si(s)+4HCl(g)△H=+240.4kJ•mol-1,生成的HCl通入100mL 1mol•L-1的NaOH溶液恰好反应,则反应过程中吸收(填“吸收”或“释放”)的热量为6.01kJ.
分析 (1)依据反应焓变△H=反应物键能总和-生成物键能总和来分析计算;
(2)太阳能电池将太阳能转化为电能;
(3)硅在自然界中含量丰富,主要以硅酸盐和二氧化硅的形式存在,仅次于氧,硅作为一种普遍使用的新型能源被开发利用说明燃烧放出的热量大,硅燃烧生成二氧化硅;
(4)通入100mL 1mol•L-1的NaOH溶液恰好反应说明生成的氯化氢为0.1mol,然后根据方程式进行计算.
解答 解:(1)已知晶体硅的燃烧热为989.2kJ•mol-1,则Si(s)+O2(g)=SiO2(s)△H=-989.2kJ•mol-1;1mol晶体硅中含有2molSi-Si,1molSiO2中含有4molSi-O,1molO2中含有1molO=O,则2×176+498.8-4x=-989.2,解得x=460,故答案为:460;
(2)硅光电池将太阳能转化为电能,太阳能热水器是将太阳能转化为内能,故答案为:光;电;
(3)A.硅常温下为固体,性质较稳定,便于贮存,较为安全,故A正确;
B.硅在自然界中含量丰富,仅次于氧,故B正确;
C.硅作为一种普遍使用的新型能源被开发利用说明燃烧放出的热量大,硅燃烧生成二氧化硅,二氧化硅是固体,容易得至有效控制,故C正确;
D.催化剂只能加快化学反应的速率,不改变反应热,故D错误;
故答案为:D;
(4)通入100mL 1mol•L-1的NaOH溶液恰好反应说明生成的氯化氢为0.1mol,设反应吸收的热量为x.
2H2(g)+SiCl4(g)═Si(s)+4HCl(g)△H=+240.4kJ•mol-1
4 240.4
0.1 x
$\frac{4}{0.1}$=$\frac{240.4}{x}$,解得x=6.01kJ,
故答案为:吸收;6.01.
点评 本题考查较为综合,涉及化学反应与能量变化以及元素化合物知识,侧重于化学与生活、生产的考查,有利于培养学良好的科学素养,提高学习的积极性,难度不大.

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案| 编号 | 热化学方程式 | 化学平衡常数 |
| ① | CO(g)+2H2(g)?CH3OH(g)△H1 | K1 |
| ② | 2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24kJ/mol | K2 |
| ③ | CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41kJ/mol | K3 |
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H-H | C≡O | C-O | H-O | C-H |
| E/(kJ/mol) | 436 | 1076 | 343 | 465 | 413 |
(2)该工艺的总反应为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H
该反应△H=-263kJ/mol,化学平衡常数K=K12•K2•K3(用含K1、K2、K3的代数式表示).
(3)下列措施中,能提高CH3OCH3产率的有AD.
A.分离出二甲醚 B.升高温度
C.改用高效催化剂 D.增大压强
(4)工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生.该工艺中反应③的发生提高了CH3OCH3的产率,原因是反应③消耗了反应②中的产物H2O,使反应②的化学平衡右移.
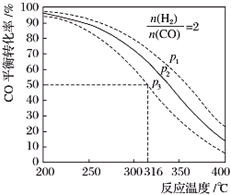
(5)以$\frac{n({H}_{2})}{n(CO)}$=2通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示.下列说法正确的是CD.
A.该反应的△H>0
B.若在p2和316℃时反应达到平衡,则CO的转化率小于50%
C.若在p3和316℃时反应达到平衡,H2的转化率等于50%
D.若在p3和316℃时,起始时$\frac{n({H}_{2})}{n(CO)}$=3,则达平衡时CO的转化率大于50%
E.若在p1和200℃时,反应达平衡后保持温度和压强不变,再充入2mol H2和1mol CO,则平衡时二甲醚的体积分数增大
(6)某温度下,将8.0mol H2和4.0mol CO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g),反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K=2.25.
| A. | 铅蓄电池属于二次电池,在充电过程中,阳极质量减小,阴极质量增加 | |
| B. | 常温下,能自发进行的反应,△H一定小于“0” | |
| C. | 一定条件下,使用催化剂能加快反应速率并提高反应物的活化能 | |
| D. | 相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 |
| A. | Na+、K+、OH-、Cl- | B. | Mg2+、Cu+、SO42-、Cl- | ||
| C. | K+、Ba2+、Cl-、HCO3- | D. | NH4+、Ba2+、Fe3+、SO42- |
(1)合金与各成分金属相比较,具有许多优良的物理,化学或机械性能
(2)相同金属元素形成的合金,元素的含量有可能不同,但其性能是相同的
(3)镁铝合金在盐酸中不能完全溶解
(4)合金具有各成分金属性质之和.
| A. | (1)(2) | B. | (1)(3) | C. | (1) | D. | (3)(4) |
| A. | 由元素X与Z形成的化合物中只含共价键 | |
| B. | XY2、ZY2、M2Y2的晶体分别属于3种不同类型的晶体 | |
| C. | 单质M的晶体是体心立方堆积,M的配位数是8 | |
| D. | X的氢化物X2H2分子中含有2个σ键和3个π键 |
| A. | 2 c1<c2 | B. | c1>c2 | C. | c1=c2 | D. | 2 c1=c2 |