题目内容
7.一定温度下,向1.0L密闭容器中加入0.60mol X(g),发生反应X(g)?Y(s)+2Z(g)△H>0,测得反应物X浓度与反应时间的数据如表:| 反应时间t/min | 0 | 1 | 2 | 3 | 4 |
| c(X)/(mol•L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 |
分析 结合v=$\frac{△c}{△t}$及速率之比等于化学计量数之比计算.
解答 解:由表格数据可知,△c(X)=0.60mol/L-0.15mol/L=0.45mol/L,则开始至4min时用X表示的平均反应速率v(X)=$\frac{0.45mol/L}{4min}$=0.1125mol•L-1•min-1,
由速率之比等于化学计量数之比可知,
开始至4min时用Z表示的平均反应速率v(Z)=0.1125mol•L-1•min-1×2=0.225 mol•L-1•min-1,
故答案为:0.225 mol•L-1•min-1.
点评 本题考查反应速率及计算,为高频考点,把握速率公式、速率与化学计量数的关系为解答关键,侧重分析与计算能力的考查,注意表格数据的应用,题目难度不大.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
2.化学在生产和生活中有重要的应用,下列说法不正确的是( )
| A. | 小苏打在生活中可用做发酵粉 | |
| B. | 硅胶可用作食品中的干燥剂 | |
| C. | 可溶性铁盐或铝盐可用于净水 | |
| D. | 二氧化硅可用于制作硅芯片和光导纤维 |
19.等质量的下列物质与足量稀硝酸反应,放出NO物质的量最少的是( )
| A. | FeO | B. | Fe2O3 | C. | FeSO4 | D. | Fe3O4 |
16. 25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )
25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )
 25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )
25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )| A. | 在上述三种盐原溶液中,水的电离程度大小是NaX>NaY>NaZ | |
| B. | 在等物质的量浓度的NaX、NaY、NaZ混合液中,离子浓度的大小关系是c(Z-)>c(Y-)>c(X-) | |
| C. | 在上述NaX和NaY的混合液中存在$\frac{c(HX)}{c({X}^{-})}$=$\frac{c(HY)}{c({Y}^{-})}$ | |
| D. | 在0.2mol•L-1 NaX溶液中加 入等体积0.1mol•L-1的盐酸,所得混合液中存在c(H+)+c(HX)=c(OH-)+c(Cl-) |
17.下列说法不正确的是( )
| A. | 将40 g NaOH溶于水配成1 L溶液,其浓度为l mol•L-1 | |
| B. | 将22.4 L HC1溶于水配成1 L溶液,其浓度为lmol•L-1 | |
| C. | 1 L含2 mol K+的K2SO4溶液中K2SO4的浓度为1mol•L-1 | |
| D. | 将浓度为0.5 mol.L-l的NaNO3溶液100 mL恒温蒸发至50 mL,其浓度变为1mol•L-1 |
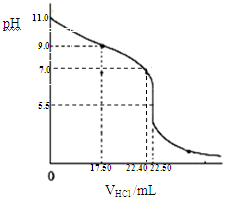 测定室温下NH3•H2O的浓度及电离平衡常数Kb
测定室温下NH3•H2O的浓度及电离平衡常数Kb