题目内容
1.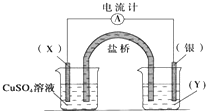 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:(1)电极X的材料是Cu,电解质溶液Y是AgNO3;
(2)银电极为电池的正极,发生的电极反应为2Ag++2e-═2Ag X电极上发生的电极反应为Cu-2e-═Cu2+.
(3)外电路中的电子是从Cu电极流向Ag电极.
分析 (1)根据电池反应式知,失电子化合价升高的金属作负极,不如负极活泼的金属或导电的非金属作正极,得电子的化合价降低的可溶性反应物作电解质溶液,据此设计原电池;
(2)原电池中,易失电子的电极铜为负极,银作正极,正极上得电子发生还原反应;
(3)电子从负极沿导线流向正极.
解答 解:(1)由反应2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)可知,在反应中,Cu被氧化,失电子,应为原电池的负极,所以X电极材料是Cu,Ag+在正极上得电子被还原,电解质溶液为AgNO3 ,
故答案为:Cu;AgNO3;
(2)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为2Ag++2e-═2Ag,X(铜)电极失电子发生氧化反应,电极反应为Cu-2e-═Cu2+,
故答案为:正极; 2Ag++2e-=2Ag;Cu-2e-═Cu2+;
(3)电子从负极Cu沿导线流向正极Ag,
故答案为:Cu;Ag.
点评 本题考查了原电池设计,明确原电池原理是解本题关键,根据电池反应式中得失电子的物质选取负极材料和电解质,知道原电池中正负极的判断方法,难度不大.

练习册系列答案
相关题目
2.下列关于有机化合物的说法正确的是( )
| A. | 2-甲基丁烷也称异丁烷 | |
| B. | 三元轴烯( )与苯互为同分异构体 )与苯互为同分异构体 | |
| C. | C4H9Cl有3种同分异构体 | |
| D. | 烷烃 的正确命名是2-甲基-3-丙基戊烷 的正确命名是2-甲基-3-丙基戊烷 |
3.下列变化只有物理变化的是( )
| A. | 荒野中出现的忽明忽暗的“天火” | |
| B. | 在低温、加压的条件下无色的气态氧变成淡蓝色的液体 | |
| C. | 固态物质在加热的条件下融化成为液体,在更高的温度下转变为气体 | |
| D. | 把棉布染上颜色 |
6.最近,国际上提出的“绿色化学”是指化学工业生产中的( )
| A. | 对废气、废水、废渣进行严格处理 | |
| B. | 在化工生产中少用或不用有害物质以及少排放或不排放有害物质 | |
| C. | 在化工生产中,不使用任何化学物质 | |
| D. | 在化工厂种草种树,使其成为花园式工厂 |
10.短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数,且X、Y、W原子最外层电子数之和恰好等于Z元素的核电荷数,X与W的最高化合价之和为8,常见金属元素Z的一种核素的质量数为28,中子数比质子数多2.下列说法中正确的是( )
| A. | Y和W的含氧酸均为强酸 | |
| B. | YW3分子中Y原子的杂化方式为sp2,分子的空间构型为平面三角形 | |
| C. | 由非金属元素组成的化合物YX5是一种是否存在尚待确证的化合物,假如存在,该物质与水反应必然生成气体X2,同时得到一种弱碱溶液 | |
| D. | 因为Z的氧化物熔点很高,不适宜于电解,故工业上常用电解Z与W的化合物的方法制取单质Z |
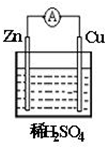 ①如图是一个原电池示意图,该原电池的负极为Zn,正极上发生还原反应.(填“氧化”或“还原”)
①如图是一个原电池示意图,该原电池的负极为Zn,正极上发生还原反应.(填“氧化”或“还原”)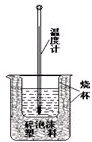 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题: