题目内容
9.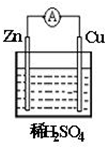 ①如图是一个原电池示意图,该原电池的负极为Zn,正极上发生还原反应.(填“氧化”或“还原”)
①如图是一个原电池示意图,该原电池的负极为Zn,正极上发生还原反应.(填“氧化”或“还原”)②电子流向:由Zn极,经导线,流向Cu极.
③它是一种把化学能转化为电能的装置
④该原电池的反应方程式为:Zn+H2SO4=ZnSO4+H2↑.
分析 锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应;铜作正极,正极上氢离子得电子发生还原反应,以此解答该题.
解答 解:①Zn较活泼,为原电池的负极,负极发生氧化反应,正极发生还原反应,故答案为:Zn;还原;
②原电池工作时,电子由负极经导线流向正极,即从Zn经导线流向Cu,故答案为:Zn;Cu;
③原电池是将化学能转化为电能的装置,故答案为:化学;电;
④该原电池的总方程式为Zn+H2SO4=ZnSO4+H2↑,故答案为:Zn+H2SO4=ZnSO4+H2↑.
点评 本题考查了原电池原理,为高频考点,侧重于双基的考查,明确正负极的判断方法即可解答,可以从电子流向、电极上得失电子、电极上发生反应类型来判断正负极,难度不大.

练习册系列答案
相关题目
10.化学与生产、生活密切相关.下列叙述正确的是( )
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 海水淡化的方法有蒸馏法、电渗析法等 | |
| C. | 棉、丝、毛、油脂都是天然有机高分子化合物 | |
| D. | 石油裂化的目的是得到乙烯、丙烯等化工原料 |
11.下列叙述中正确的是( )
| A. | 标准状况下,40gSO3的体积约为11.2L | |
| B. | 硫粉在过量的纯氧中燃烧生成SO3 | |
| C. | 使用清洁能源是防止酸雨发生的重要措施之一 | |
| D. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
8.粉笔具有吸附性,不同物质在粉笔表面具有不同的附着能力.用洁净的白粉笔、水进行层析实验,可以分离红、蓝墨水混合液中的染料.该实验的过程如图所示:
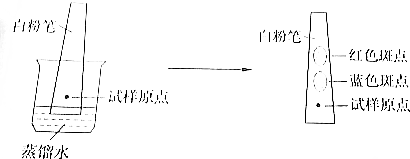
分析以上信息,可知该实验中蒸馏水( )

分析以上信息,可知该实验中蒸馏水( )
| A. | 是固定相 | B. | 是流动相 | ||
| C. | 是惰性支持物 | D. | 既是固定相,又是流动相 |
 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: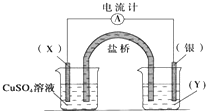 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题: